
SO2����������Fe2��SO4��3��Һ��ȫ��Ӧ���ټ���K2Cr2O7��Һ����������������ѧ��Ӧ����SO2��2Fe3����2H2O===SO42-��2Fe2����4H����
��Cr2O72-��6Fe2����14H��===2Cr3����6Fe3����7H2O��
�����й�˵���������
A�������ԣ�Cr2O72->Fe3��>SO2
B��K2Cr2O7�ܽ�Na2SO3������Na2SO4
C��ÿ��1 mol K2Cr2O7�μӷ�Ӧ��ת�Ƶ��ӵ���ĿΪ6NA
D������6.72 L SO2����״�����μӷ�Ӧ������������0.2 mol K2Cr2O7
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ��10�µ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�����Һ�п��Է�����Ӧ��X+2Y3+�TX2++2Y2+�������н��ͣ���X����������X������������X���л�ԭ�ԣ���Y2+�����������Y2+���л�ԭ�ԣ���Y3+�������Ա�X2+Ҫǿ��������ȷ����
A���ڢܢ� B���٢ۢ� C���ڢ� D���٢ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�����и�����ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��12�֣������������ѵ���Ҫ������Ѱף������Ķ������ѣ���һ�������ʸߡ���ɫ�����ڸ���ǿ����ѧ�����ȶ��İ�ɫ���ϡ�����������Ҫ�ɷ�FeTiO3����Fe2O3��SiO2�����ʣ���ȡ�������ѣ��������ᷨ�����������£�
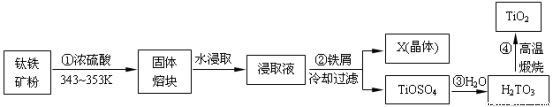
��1����������Ҫ�ɷ���Ũ���ᷴӦ����Ҫ������TiOSO4��FeSO4���÷�Ӧ�Ļ�ѧ����ʽΪ
��2��Ϊ��ߡ������ۿ顱ˮ��ȡʱ�Ľ����ʣ����˲���ѭ����ȡ���ӳ�ʱ���⣬���˵�����������ѡ�� ��
��3����ȡҺ����м��Ӧ�����ӷ���ʽΪ ��X�����壩Ϊ�̷���FeSO4��7H2O�������ơ��������Һʱ���������м��Ŀ���� ��
��4������ʱ���貣������Ϊ �� ���ձ���
��5���ڢ۲���Ӧ��ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڱ�״���£���aLNH3��ȫ����ˮ�õ�VmL��ˮ����Һ���ܶ�Ϊ��g��cm��3�����ʵ���������Ϊ�أ����ʵ����ʵ���Ũ��Ϊcmol/L��������������ȷ����
�٦أ� ��c��
��c��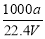
��������Һ���ټ���VmLˮ��������Һ��������������0��5��
��������Һ���ټ���1��5VmLͬŨ��ϡ���ᣬ��ַ�Ӧ����Һ������Ũ�ȴ�С��ϵΪ��
c��Cl������c��NH4+����c��H+����c��OH����
A���٢� B���ڢ� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����и�����ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��1mol Na2CO3�ı�����Һ�л���ͨ��CO2����ʹ֮��ַ�Ӧ������ͼ���ʾ��ȷ����
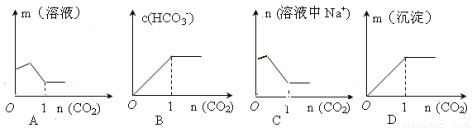
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ������ѧ�ڶ���ģ��������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¿����������ӣ�Na+��NH4+��Mg2+��Al3+��SO42����NO3����Cl�� ��ijͬѧ�ռ��˸õ���������������Ҫ��Ԥ�������������Һ����Ʋ���������µ�ʵ�飺
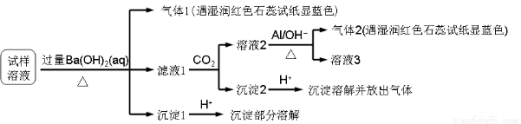
��֪��3NO3�� + 8Al + 5OH�� + 2H2O = 3NH3 + 8AlO2��
�������ϵ�ʵ�����������ͬѧ�ó��Ľ��۲���ȷ����
A�������п϶�����NH4+��Mg2+��SO42����NO3��
B���������п��ܴ���NaNO3 ��NH4Cl��MgSO4
C�������п��ܴ���Na+��Cl��
D��������һ������Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Ԫ��X��Y��Z��W��Q��ԭ��������������Yԭ�ӵĺ�����������ڲ���ӵ�4����X����̬�⻯�K������Y���⻯���У������£�Z�ĵ���������W������������ˮ�����ϡ��Һ��ȴ��������Ũ��Һ������˵������ȷ����
A��Ԫ��Q������������Ӧ��ˮ�������Ա�W��ǿ
B��������W2Q2�У���ԭ����������8���ӽṹ
C����ҵ��ͨ�����Z��Q�γɵĻ������Ʊ�Z����
D��Y������X����̬�⻯��ɷ����û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ�����и�����ѧ�ڵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��CO��g����ȼ���ȣ���H=-283��0KJ/mol,��2CO2��g��=2CO��g��+O2��g����Ӧ�ġ�H=-556��0KJ/mol
B����֪NaOH��aq��+HCl��aq��=NaCl��aq��+H2O��l�� ��H=-57��30KJ/mol-1,��40��0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�57��3KJ������
C����֪2C��s��+2O2��g��=2CO2��g�� ��H=a; 2C��s��+O2��g��=2CO��g��; ��H=b, ��a��b
D����֪c��ʯī��s��=C�����ʯ��s�� ��H��0,��ʯī�Ƚ��ʯ�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ�ڿ�ѧ������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�鷽��������ͽ��۾���ȷ����
ѡ�� | ʵ�鷽�� | ���� | ���� |
A |
| �����ƻ���ʱ������©������һ��ˮ������ֹ��ˮ���߶Ȳ��� | ��װ�õ����������� |
B |
| ��֬��ȼ�� | Na2O2��ˮ��Ӧ�����������ƺ����� |
C |
| �ձ��ٵij���ʯ��ˮ�ȱ���� | NaHCO3��Na2CO3���ȸ��ֽ� |
D |
| U�ι��Ҷ˵�Һ��� | ��������������ʴ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com