��һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϣ�
��1���������з�Ӧ���Խ�����ת��Ϊ���ȴ�99.9%�ĸߴ�����
Ni��s��+4CO��g��

Ni��CO��
4��g�� �÷�Ӧ�ġ�H
��
��
0 ��ѡ�������=����������
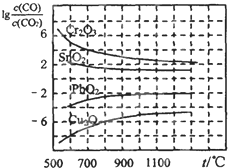
��2���ڸ�����һ����̼�ɽ���������ԭΪ��������֪��
C��s��+O
2��g��=CO
2��g����H
1=-393.5kJ?mol
-1CO
2��g��+C��s��=2CO��g����H
2=+172.5kJ?mol
-1S��s��+O
2��g��=SO
2��g����H
3=-296.0kJ?mol
-1���CO��SO
2���Ȼ�ѧ����ʽ
2CO��g��+SO2��g��=S��s��+2CO2��g����H3=-270kJ?mol-1
2CO��g��+SO2��g��=S��s��+2CO2��g����H3=-270kJ?mol-1
��
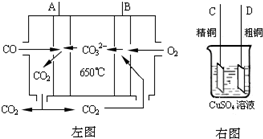
��3����ͼ����ͼ��һ̼����ȼ�ϵ�أ�����COΪȼ�ϣ�һ������Li
2CO
3��Na
2CO
3���ۻ����Ϊ����ʣ���ͼ�Ǵ�ͭ������װ��ͼ������ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飮�ش��������⣺
��д��A�������ĵ缫��Ӧʽ
CO-2e-+CO32-=2CO2
CO-2e-+CO32-=2CO2
��
��Ҫ��ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飬��B��Ӧ����
D
D
�� �����C����D����������
�۵�����2.24L������£�COʱ����ͭ�缫�����ϼ���ͭ������
��
��
��������ڡ��������ڡ���С�ڡ���6.4�ˣ�
��1����֪Na
2CrO
4��Һ�ữʱ�����ķ�ӦΪ��2CrO
42-+2H
+?Cr
2O
72-+H
2O����1L�ữ��������Һ�и�Ԫ�ص������ʵ���Ϊ0.55mol��CrO
42-��
ת��ΪCr
2O
72-����֪������ʱ�÷�Ӧ��ƽ�ⳣ��K=10
14�������ữ��������Һ��pH=
6
6
��
��2�������йع��ұ�����CrO
42-�ķ�ˮҪ����ѧ������ʹ��Ũ�Ƚ���5.0��10
-7mol?L
-1���²����ŷţ���CrO
42-�ķ�ˮ����ͨ�����������ַ�����
�ٳ���������������Ա�������BaCrO
4����[K
sp��BaCrO
4��=1.2��10
-10]���ټ�������������δ��������Ba
2+����������Ա��κ�ķ�ˮ��Ba
2+��Ũ��Ӧ��С��
2.4��10-4
2.4��10-4
mol?L
-1��Ȼ���ٽ��к����������ܴﵽ�����ŷű���
�ڻ�ԭ����CrO
42-Cr
3+Cr��OH��
3���ø÷�������10m
3 CrO
42-�����ʵ���Ũ��Ϊ1.0��10
-3 mol?L
-1�ķ�ˮ��������Ҫ�̷���FeSO
4?7H
2O����Է�������Ϊ278��
8.34
8.34
Kg��������λС������




 Ni��CO��4��g�� �÷�Ӧ�ġ�H
Ni��CO��4��g�� �÷�Ӧ�ġ�H
 һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϣ�
һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϣ� Ni��CO��4��g�� �÷�Ӧ�ġ�H
Ni��CO��4��g�� �÷�Ӧ�ġ�H