
【题目】在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.硫酸中逐滴加入氢氧化钡溶液
D.醋酸中逐滴加入氨水(一水合氨为弱电解质,CH3COONH4为强电解质)
【答案】C
【解析】
A. HCl是强电解质,在水溶液里完全电离,加入NaCl后,二者不反应,溶液中电荷浓度不是0,所以不熄灭,故A错误;
B. 硫酸和NaOH都是强电解质,二者发生反应H2SO4+2NaOH=Na2SO4+H2O,生成的硫酸钠是强电解质,溶液中离子浓度减小,所以灯泡变暗,但不熄灭,故B错误;
C. 硫酸和氢氧化钡都是强电解质,二者发生反应Ba(OH)2+H2SO4=BaSO4↓+2H2O,反应后生成难溶物和弱电解质,溶液中离子浓度逐渐减小,所以灯泡变暗,二者恰好反应时离子浓度最小,灯泡熄灭,再继续滴加氢氧化钡,溶液中离子浓度增大,灯泡变亮,符合题意,故C正确;
D. 醋酸、一水合氨都为弱电解质,二者反应生成醋酸铵,溶液导电性增强,不存在熄灭的现象,故D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式____________________,氧化产物与还原产物的物质的量之比为_______。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_____ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_________________(用文字表达),又变为棕黄色的离子方程式是_____________________。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474 g KMnO4样品溶解酸化后,用0.100 mol·L-1标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在___(填“酸式”或“碱式”)滴定管中。配平上述反应的离子方程式:___MnO4-+___S2O32-+____H+=____Mn2++_____SO42-+____H2O,实验中,滴定至终点时消耗Na2S2O3溶液12.00 mL,则该样品中KMnO4的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
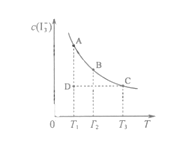
【题目】I2在KI溶液中存在平衡:I2(aq)+I-(aq)![]() I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的平衡曲线图如下。下列说法不正确的是
I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的平衡曲线图如下。下列说法不正确的是
A.反应I2(aq)+I-(aq)![]() I3-(aq)的△H>0
I3-(aq)的△H>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C.若反应进行到状态D时,一定有![]()
D.状态A与状态B相比,状态A的c (I2) 小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用不同的实验装置研究苯与液溴的反应并制取少量溴苯。试回答下列问题:


(1)若采用图甲装置进行实验,装置A中应预先需加入的试剂是____,E装置的作用是___。
(2)若采用图乙装置进行实验,C中盛放的CCl4的作用是____________。
(3)若使用图乙装置,实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,然后用___(填仪器名称)分离出溴苯(仍含有少量苯)。写出有关的离子反应方程式__________。
(4)反应完毕后,向试管D中滴加AgNO3溶液,若有_______(填现象)生成,说明这种获得溴苯的反应属于______ (填有机反应类型)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将1molH2和1molI2的气态混合物充入1L的密闭容器中,发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH<0;5 min后达到平衡状态,测得c(H2)=0.9mol·L-1,则下列结论中,不能成立的是( )
2HI(g) ΔH<0;5 min后达到平衡状态,测得c(H2)=0.9mol·L-1,则下列结论中,不能成立的是( )
A.平衡时H2、I2的转化率相等
B.从反应开始至平衡的过程中,v(HI)=0.04mol·L-1·min-1
C.其他条件不变再向容器中充入少量H2,I2的转化率提高
D.若将容器温度提高,其平衡常数K一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法正确的是( )
A. 取等体积、同浓度的醋酸和盐酸溶液与足量Zn反应,产生的氢气量一样多。
B. 用HF溶液做导电性实验,灯泡很暗,则一定说明HF为弱电解质。
C. 稀释醋酸溶液,溶液中所有离子浓度都减少。
D. 氨水稀释时,![]() 不断减少
不断减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将尿酸钠(![]() )悬浊液静置,取上层清液,再通入
)悬浊液静置,取上层清液,再通入![]() ,溶液中尿酸的浓度
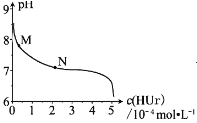
,溶液中尿酸的浓度![]() 与
与![]() 的关系如图所示。己知:
的关系如图所示。己知:![]() ,
,![]() ,下列说法正确的是
,下列说法正确的是
A. 上层清液中,![]()
B. 当![]() 时,
时,![]()
C. 在![]() 的变化过程中,c(Na+) ·c(Ur-)的值将逐渐减小
的变化过程中,c(Na+) ·c(Ur-)的值将逐渐减小
D. 当![]() 时,
时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生反应A(s)+2B(g)![]() C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述中错误的是
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述中错误的是
A. 在5 min内该反应用C的浓度变化表示的反应速率为0.02 mol/(Lmin)
B. 5 min时,容器内D的浓度为0.2 mol/L
C. 该可逆反应随着反应的进行,容器内压强逐渐增大
D. 5 min时,容器内气体总的物质的量为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Ba(OH)2·8H2O固体与NH4Cl固体反应的化学方程式为_____________。
(2)拆开1 mol H—H键,1 mol N—H键,1 mol N≡N键分别需要吸收的能量为436 kJ,391 kJ,946 kJ。理论上,每生成1 mol NH3___________热量(填“吸收”或“放出”)__________kJ;事实上,反应的热量总小于理论值,为什么?________________。
(3)一定条件下发生反应:6NO(g) + 4NH3(g)![]() 5N2(g) + 6H2O(g),某次实验中测得容器内NO及N2的物质的量随时间变化如下图甲所示,图中b点对应的速率关系是v(正) _____ v(逆) ; d点对应的速率关系是v(正) ___________ v(逆)。(填“﹥”、“﹤”或“﹦”)
5N2(g) + 6H2O(g),某次实验中测得容器内NO及N2的物质的量随时间变化如下图甲所示,图中b点对应的速率关系是v(正) _____ v(逆) ; d点对应的速率关系是v(正) ___________ v(逆)。(填“﹥”、“﹤”或“﹦”)

(4)已知N2(g)+ 3H2(g) ![]() 2NH3(g),若反应起始时N2、H2 、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.1 mol/L,则NH3达到平衡时浓度的范围为_______;若平衡时N2、H2 、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.1 mol/L,则NH3起始时浓度的范围为______。
2NH3(g),若反应起始时N2、H2 、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.1 mol/L,则NH3达到平衡时浓度的范围为_______;若平衡时N2、H2 、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.1 mol/L,则NH3起始时浓度的范围为______。
(5)已知一定条件下发生:2SO2(g) + O2(g) ![]() 2SO3(g) (正反应放热),在反应过程中,正反应速率的变化如图所示,请根据速率的变化回答采取的措施(改变的条件)
2SO3(g) (正反应放热),在反应过程中,正反应速率的变化如图所示,请根据速率的变化回答采取的措施(改变的条件)

t1________________________;t2________________________;
t3________________________;t4________________________。
(6)①某电池采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液,电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中_______作正极,负极的电极反应为_________________。
②甲烷燃料电池示意图如上图乙,其负极反应方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com