
| A. | 1mol NH4+ 含有的电子总数为10NA | |
| B. | 1mol Mg 与足量盐酸反应时失去NA个电子 | |
| C. | 28g N2 所含原子数目为NA | |
| D. | 在101KPa、25℃条件下,11.2L H2 中含有的原子数目为NA |
分析 A.铵根离子中含有10个电子,1mol铵根离子中含有10mol电子;
B.每个镁原子失去两个电子;
C.氮气是双原子分子,28g氮气的物质的量是1mol,含有2mol氮原子;
D.常温常压下,不是标准状况下.
解答 解:A.1molNH4+含有10mol电子,含有的电子数为10NA,故A正确;
B.因为每个镁原子失去两个电子,则1molMg与足量盐酸反应时失去2NA个电子,故B错误;
C.28g氮气的物质的量是1mol,含有2mol氮原子,所含的原子数目为2NA,故C错误;
D.常温下,不能使用标况下的气体摩尔体积计算11.2LH2的物质的量,故D错误.
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确分子、原子、原子核内质子中子及核外电子的构成关系;D为易错点,注意标准状况下气体摩尔体积为22.4L/mol.


科目:高中化学 来源: 题型:选择题
| A. | 46 | B. | 34 | C. | 30 | D. | 60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰氧化钙可用作食品的防氧化剂 | |
| B. | P2O5不可用作食品干燥剂 | |
| C. | 无水硅胶可用作食品干燥剂 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅是构成一些岩石和矿物的基本元素 | |
| B. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| C. | 高纯度的二氧化硅用于制作光导纤维 | |
| D. | 陶瓷是人类应用很早的硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在7.8gNa2O2晶体中阳离子与阴离子总数为0.3NA | |
| B. | 在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 | |
| C. | 1mol Na2O2与H2O完全反应,转移的电子总数为NA | |
| D. | 在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
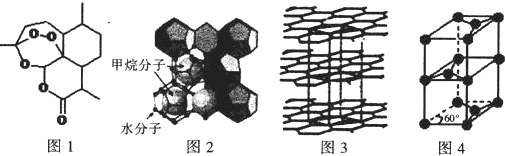
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:NH4+、Ag+、PO43-、Cl- 能大量共存 | |
| B. | 水电离产生的c(H+)=10-12 mol•L-1的溶液:K+、Ba2+、Cl?、Br-一定能大量共存 | |
| C. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-能大量共存 | |
| D. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 LCl2分别与铁和铜反应时,失电子数目均为NA | |
| B. | 1mol Na2O2与CO2足量反应时,转移NA个电子 | |
| C. | 12.0gNaHSO4固体中含有的阳离子数目为0.2NA | |
| D. | 1mol Na2O2晶体中含有的阴离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、植物油和苯都能与氢气发生加成反应,是因为其结构中都含有碳碳双键 | |
| B. | 开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 | |
| C. | 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 | |
| D. | 制造玻璃是复杂的物理变化,玻璃的组成不同,性能不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com