
| A.250mL | B.425mL | C.500mL | D.560mL |
科目:高中化学 来源:不详 题型:单选题
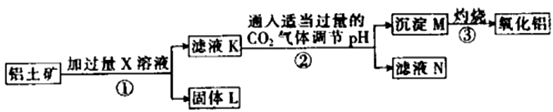
| A.X既可以是HCl,也可以是NaOH |
B.第②步反应的离子方程式为: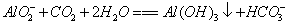 |
| C.固体L中含有SiO2、Fe2O3和MgO等 |
| D.滤液N经蒸发结晶后可以得到纯净的Na2CO3固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④⑤ | B.①⑤ | C.①②③ | D.①④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8.9g | B.9.0g | C.13.5g | D.27.0g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
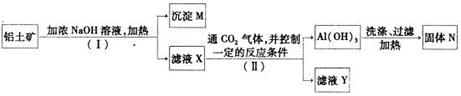
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下与足量18mol/LH2SO4反应,最多可放出0.6 mol H2 |
| B.常温下与足量2mol/LHNO3反应,最少可放出0.45 mol H2 |
| C.常温下与足量2 mol/L H2SO4反应,放出H2的量在0.45 mol~0.6 mol之间 |
| D.常温下与足量2mol/LNaOH反应,放出H2的量在0.45 mol~0.6 mol之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 经过滤、洗涤、干燥得沉淀质量为5.24克
经过滤、洗涤、干燥得沉淀质量为5.24克查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com