
����Ŀ��A��MΪ��ѧ��ѧ�ij������ʣ�����֮���ת����ϵ��ͼ��ʾ������������ͷ�Ӧ����ʡ�ԣ���֪C��D����Ԫ��X��Y��Z�е�������ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�����Ҳ���ȼ�գ�GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ�ٳ���������ӡˢ��·�壮��ش��������⣺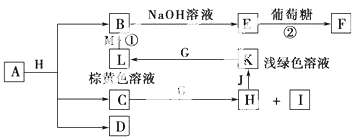
��1��д��A�Ļ�ѧʽ�� ��
��2���Ƚ�Y��Z��ԭ�Ӱ뾶��С��������Ԫ�ط��ţ���
��3������L��Һ�н��������ӵķ����� ��
��4����֪F����ϡ���ᣬ��Һ�����ɫ���ų���ɫ���壮��д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1��CuCO3��Cu��OH��2��CO3��2
��2��C��O
��3��ȡ����L��Һ���Թ��У��μ�KSCN��Һ������Һ��Ѫ��ɫ��֤������Fe3+
��4��3Cu2O+14HNO3��ϡ��=6Cu��NO3��2+2NO��+7H2O
���������⣺��֪C��D����Ԫ��X��Y��Z�е�������ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С����XΪHԪ�أ�Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�����Ҳ���ȼ�գ�DΪCO2 �� YΪCԪ�ء�ZΪOԪ�أ�LΪ�ػ�ɫ��Һ����L�к���Fe3+ �� KΪdz��ɫ��Һ����K�к���Fe2+ �� GΪ����ɫ�������壬��GΪCl2 �� ��LΪFeCl3 �� KΪFeCl2 �� ��Ӧ�ٳ���������ӡˢ��·�壬�����MΪCu��BΪCuCl2 �� EΪFe��OH��2 �� FΪCu2O����������C��Ӧ����H��H�����J��Ӧ�õ�FeCl2 �� ��HΪHCl��I��Ư�����ã�����IΪHClO��CΪˮ����AΪCuCO3��Cu��OH��2��CO3��2 �� ��1��A�Ļ�ѧʽ��CuCO3��Cu��OH��2��CO3��2 �� ���Դ��ǣ�CuCO3��Cu��OH��2��CO3��2����2��YΪCԪ�أ�ZΪOԪ�أ�ԭ�Ӱ뾶C��O�����Դ��ǣ�C��O����3������L��FeCl3����Һ�н��������ӵķ����ǣ�ȡ����L��Һ���Թ��У��μ�KSCN��Һ������Һ��Ѫ��ɫ��֤������Fe3+ �� ���Դ��ǣ�ȡ����L��Һ���Թ��У��μ�KSCN��Һ������Һ��Ѫ��ɫ��֤������Fe3+ �� ��4��F��Cu2O������ϡ���ᣬ��Һ�����ɫ���ų���ɫ���壬��Ӧ��������ͭ��NO��ˮ����Ӧ�Ļ�ѧ����ʽ��3Cu2O+14HNO3��ϡ��=6Cu��NO3��2+2NO��+7H2O��
���Դ��ǣ�3Cu2O+14HNO3��ϡ��=6Cu��NO3��2+2NO��+7H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦmA���̣�+nB������Pc ������+qD��������Ӧ������������������ʱC�İٷֺ���C%���¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��������������ȷ���ǣ� �� 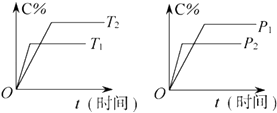
A.�ﵽƽ���ʹ�ô�����C%������
B.�ﵽƽ����������¶ȣ���ѧƽ�����淴Ӧ�����ƶ�
C.����ʽ��n��p+q
D.�ﵽƽ�������A���������ڻ�ѧƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���������˵����ȷ����
A.����������ɫ����B.����������ˮ����
C.��ʹ����ĺ�ɫ������ɫD.H2��Cl2��ȼ�գ�����ʵ���ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������������ԭ��Ӧ����
A. Cl2��2KBr=Br2��2KCl
B. 2NH4Cl + Ca(OH )2![]() CaCl2 +2NH3��+ 2H2O
CaCl2 +2NH3��+ 2H2O
C. 3Mg��N2![]() Mg3N2
Mg3N2
D. 2Na2O2��2CO2=2Na2CO3��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ƕ�ֲ����������ȱ�ٵ�Ԫ�أ�����������Ҳ����Ҫ�Ļ���ԭ�ϡ���Ȼ���д�������ͼ��ʾ�ĵ�Ԫ�ص�ѭ�����̣�����˵������ȷ����
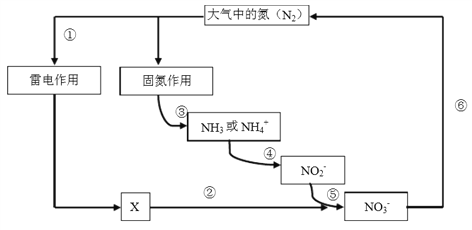
A. ���̢١������á��з����ķ�Ӧ�ǣ�N2 + O2 === 2NO
B. ���̢� ���̵����á��У���������ԭ
C. �����漰�ķ�Ӧ�����У� 2 NO2 + O2 === 2 NO3
D. �����漰�ķ�Ӧ�����У� 2NO3- + 12H+ === N2+ 6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A�ǻ����B�ǽ������ʣ�����֮�����Ӧ�Լ�������֮���ת����ϵ��ͼ��ʾ��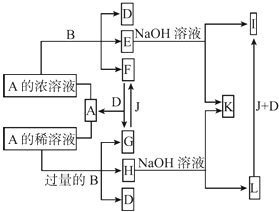
��1������B��Ԫ�����ڱ��е�λ���� �� B��A��Ũ��Һ��Ӧ�������� �� д������B��A��ϡ��Һ��Ӧ�����ӷ���ʽ�� ��
��2��������0.1 mol/L E��ˮ��Һ�и�����Ũ�ȴ�С��ϵΪ ��
��3��Lת��ΪI�������� �� д���йصĻ�ѧ����ʽ�� ��
��4����μ��H��Һ�������ӵĴ��ڣ�д��ʵ����������������ۣ� ��
��5����֪25��ʱFe��OH��3��Ksp=3.5��10��39 �� �ֽ�4.0��10��8 mol/L E��Һ��2.0��10��8 mol/L NaOH��Һ�������ϣ�������Һ���ʱ����ı仯����ͨ����ʽ����˵���Ƿ��г��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ס��ҡ�����X��4����ѧ��ѧ�г��������ʣ���ת����ϵ������ͼ�����ֲ�������ȥ��������˵���У���ȷ���ǣ� �� 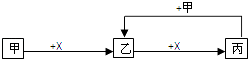
A.����Ϊ�����������һ��ΪFeCl3
B.����Ϊǿ���Xһ��ΪCO2
C.������һ�ְ�ɫ��״�����������Һ��һ������Al3+
D.����Ϊ���ʣ���˹�ϵ���漰�ķ�Ӧһ������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̽��С�����ñ�ͪ�������Ӧ��CH3COCH3+Br2 ![]() CH3COCH2Br+HBr�����о���Ӧ��Ũ���뷴Ӧ���ʵĹ�ϵ����Ӧ����v��Br2��ͨ���ⶨ�����ɫ��ʧ�����ʱ����ȷ������һ���¶��£��������ʵ�����ݣ�
CH3COCH2Br+HBr�����о���Ӧ��Ũ���뷴Ӧ���ʵĹ�ϵ����Ӧ����v��Br2��ͨ���ⶨ�����ɫ��ʧ�����ʱ����ȷ������һ���¶��£��������ʵ�����ݣ�
ʵ����� | ��ʼŨ��c/molL��1 | ����ɫ��ʧ�����ʱ��t/s | ||
CH3COCH3 | HCl | Br2 | ||
�� | 0.80 | 0.20 | 0.0010 | 290 |
�� | 1.60 | 0.20 | 0.0010 | 145 |
�� | 0.80 | 0.40 | 0.0010 | 145 |
�� | 0.80 | 0.20 | 0.0020 | 580 |
����ʵ���������ó��Ľ��۲���ȷ���ǣ� ��
A.����c��CH3COCH3����v��Br2������
B.ʵ��ں͢۵�v��Br2�����
C.����c��HCl����v��Br2������
D.����c��Br2����v��Br2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�к���Mg2+��Al3+��Fe3+��Cu2+��NH4+��Na+�е�һ�ֻ��֣�ȡ100mL����Һ�������в��ϵμ�NaOH��Һ�������ij�������NaOH����仯�Ĺ�ϵ��ͼ��ʾ����������������ȷ����
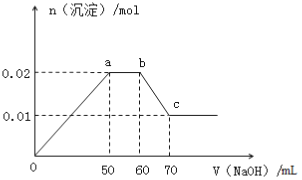
A. ����Һ��һ������Fe3+��Cu2+
B. ����Һ��һ������Mg2+��Al3+��NH4+�����������ʵ���Ũ��֮��Ϊ1:1:2
C. ����NaOH��Һ���ʵ���Ũ��Ϊ1mol/L
D. a�㵽b�㣬NH4++OH- =NH3��H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com