
【题目】今有Ba(NO3)2、AgNO3、Fe(NO3)3的混合液。欲将Ba2+、Ag+、Fe3+分离,分别得到三种元素的不溶物,按下图所示实验:
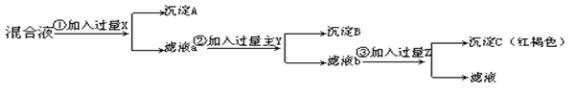
⑴加入的试剂分别是:X________,Y_________,Z_________。
⑵生成的沉淀A是__________,B是___________,C是___________。
⑶第②步和第③步的离子方程式分别是________________________________________________。
【答案】盐酸 硫酸 氢氧化钠溶液 AgCl BaSO4 Fe(OH)3 Ba2++SO42-==BaSO4↓ H++OH-=H2O Fe3++3OH-=Fe(OH)3↓
【解析】
依据物质溶解度和流程可知,先加入盐酸沉淀银离子,过滤后加入稀硫酸沉淀钡离子,最后加入强碱沉淀铁离子,据此解答。
(1)沉淀钡离子一般用硫酸根离子,沉淀银离子一般用氯离子,沉淀铁离子一般用氢氧根离子,由于硫酸银微溶于水,所以首先沉淀银离子,即X是HCl,根据流程图可知最后得到红褐色沉淀,则Y是H2SO4,用来沉淀钡离子,Z是NaOH,用来沉淀铁离子,即加入的试剂X、Y、Z分别是盐酸、硫酸、氢氧化钠溶液。
(2)根据以上分析可知生成的沉淀A、B、C分别是是AgCl、BaSO4、Fe(OH)3。
(3)根据以上分析可知反应第②步的离子方程式是Ba2++SO42-=BaSO4↓。由于前面加入的硫酸是过量的,则第③步的离子方程式为H++OH-=H2O、Fe3++3OH-=Fe(OH)3↓。


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KC1O3和草酸(H2C2O4)在60℃时反应制得。某学生用下图所示的装置模拟工业制取及收集C1O2,其中A为C1O2的发生装置,B为C1O2的凝集装置,C为尾气吸收装置。
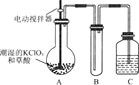
请回答下列问题:
(1)A中反应产物有K2CO3、C1O2和CO2等,请写出该反应的化学方程式:________________________。
A部分还应添加温水浴控制温度在60 °C,B部分还应补充什么装置:_________________。
(2)该装置按(1)补充完整后,装置A、B、C中还有一处设计明显不合理的是_____(填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),该反应的离子方程式为____________。若实验时需要450 mL 4 mol L-1的NaOH溶液,则在精确配制时,需要称取NaOH的质量是____g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列物质分类全部正确的是( )
①苏打 ②食盐水 ③石灰水 ④NaOH ⑤液氧 ⑥KClO3
A.纯净物—③④⑤B.混合物—②⑤
C.盐—①⑥D.碱—①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出),单质A常作为食品包装材料,甲是两性氧化物。
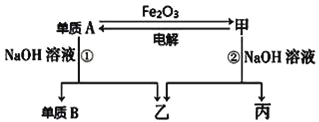
根据图示转化关系回答:
(1)写出反应①的离子方程式:_________________。
(2)实验室完成单质A与Fe2O3反应实验,需要的试剂还有_______。
a.KCl b.KClO 3 c.MnO2 d.Mg
(3)利用该反应的原理,工业上可用于___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中粒子的物质的量浓度关系正确的是
A. 0.1 mol·L-1 Na2CO3与0.l mol·L-1 NaHCO3溶液等体积混合:2/3 c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3)
B. 0.1 mol·L-1 Na2C2O4与0.1 mol·L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
C. 0.1 mol·L-1 CH3COONa与0.l mol·L-1 HCl 溶液等体积混合:c(Na+) = c(Cl-) > c(OH-) > c(CH3COO-)
D. 0.l mol·L-1 NH4Cl与0.l mol·L-1氨水等体积混合(pH > 7): c(NH3·H2O) > c(NH4+) > c(Cl-) > c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如表提供的数据可知,在溶液中能大量共存的微粒组是

A. H2CO3 、HCO3-、CH3COO-、CN-
B. CO32-、 HCO3-、CH3COOH、CN-
C. HCO3-、CH3COO-、CN-、HCN
D. HCN 、HCO3-、CN-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1 mol A、2 mol B,此时甲、乙的容积均为2 L(连通管体积忽略不计)。在T℃时,两容器中均发生下述反应:A(g)+2B(g)![]() 2C(g)+3D(g) △H < 0。达平衡时,乙的体积为2.6 L,下列说法正确的是
2C(g)+3D(g) △H < 0。达平衡时,乙的体积为2.6 L,下列说法正确的是
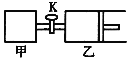
A. 甲中反应的平衡常数小于乙
B. 若打开活塞K,达平衡时乙容器的体积为3.2 L
C. 当乙中A与B的体积分数之比为1:2时,反应达到平衡状态
D. 平衡时甲容器中A的物质的量小于0.55 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内含量虽然很少,却是维持正常生命活动不可缺少的。这可通过下面的哪一实例得到证实( )
A.缺Mg时叶片变黄
B.油菜缺B时只开花不结果
C.动物血液中钙盐的含量太低会抽搐
D.缺P会导致作物植株矮小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.Mg2+、K+、OH﹣B.Ba2+、Na+、SO42﹣
C.K+、NH4+、OH﹣D.K+、Cu2+、NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com