
【题目】有机物丙是一种香料,其合成路线如图。

已知![]()
乙与苯甲醇(![]() )互为同系物,丙分子中只有两个甲基。
)互为同系物,丙分子中只有两个甲基。
(1)A的分子式是![]() ,分子中有支链,则A的结构简式是__________________;
,分子中有支链,则A的结构简式是__________________;
(2)C和新制![]() 悬浊液反应的化学方程式是____________________________;
悬浊液反应的化学方程式是____________________________;
(3)D能发生银镜反应,分子式为![]() 。
。![]() 与
与![]() 反应,最多消耗_________
反应,最多消耗_________ ![]() ;
;
(4)甲和乙反应生成丙的化学方程式是________________________;
(5)乙的同分异构体中,显弱酸性且苯环上有2个取代基的共有_________种。
【答案】 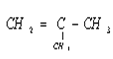
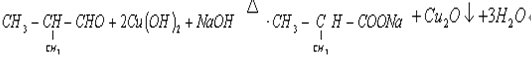 5
5 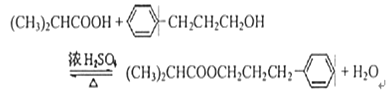 6
6
【解析】乙与苯甲醇互为同系物,则乙为醇,甲为羧酸,二者发生酯化反应生成丙,由A的分子式是C4H8,分子中有支链,根据A生成B的反应条件和题中信息以及B能经过两步氧化得甲,可知A为(CH3)2C=CH2,所以B为(CH3)2CHCH2OH,C为(CH3)2CHCHO,甲为(CH3)2CHCOOH,根据丙的分子式和乙为醇,以及丙分子中有两个甲基,可推知乙为![]() ,D能发生银镜反应,所以D为
,D能发生银镜反应,所以D为![]() ,根据甲和乙可推知,丙为
,根据甲和乙可推知,丙为![]() ,则
,则
(1)根据上面的分析可知,A的结构简式是(CH3)2C=CH2;(2)C为(CH3)2CHCHO,C和新制Cu(OH)2悬浊液反应的化学方程式为(CH3)2CHCHO+2Cu(OH)2+NaOH![]() (CH3)2CHCOONa+Cu2O↓+3H2O;(3)D为
(CH3)2CHCOONa+Cu2O↓+3H2O;(3)D为![]() ,1molD与H2反应,最多消耗5 molH2;(4)甲和乙反应生成丙的化学方程式为:(CH3)2CHCOOH+
,1molD与H2反应,最多消耗5 molH2;(4)甲和乙反应生成丙的化学方程式为:(CH3)2CHCOOH+![]()
![]()
![]() +H2O;(5)乙为
+H2O;(5)乙为![]() ,其同分异构体符合:显弱酸性且苯环上有2个取代基,则侧链为-OH、-CH2CH2CH3,或侧链为-OH、-CH(CH3)2,各有三种邻、间、对三种结构,所以共有6种。
,其同分异构体符合:显弱酸性且苯环上有2个取代基,则侧链为-OH、-CH2CH2CH3,或侧链为-OH、-CH(CH3)2,各有三种邻、间、对三种结构,所以共有6种。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列陈述I、II正确并且有因果关系的是 ( )
选项 | 陈述I | 陈述II |
A | 铝可以分别和NaOH溶液、盐酸反应 | 铝既有金属性又有非金属性 |
B | Na2CO3可以制胃药 | Na2CO3可以和盐酸反应 |
C | 硬铝是合金 | 其熔点比金属铝的熔点高 |
D | Na2O2具有强氧化性 | Na2O2可以作为漂白剂 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖分解代谢的叙述,错误的是
A. 甜菜细胞中的蔗糖经水解可产生葡萄糖和果糖
B. 各种糖类都可以氧化分解,为细胞供能
C. 发芽小麦种子中的麦芽糖经水解可产生葡萄糖
D. 纤维素经微生物水解可产生葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,硫的某种含氧酸H2SOx(x≤4)与H2S可发生如下反应:H2S+H2SOx—S+(x-3)SO2+H2O(未配平)下列推断合理的是
A. 该反应中,一定有SO2 B. 该反应中,H2S作还原剂,H2SOx作氧化剂
C. 若x=3,则还原剂与氧化剂的物质的量之比为1:1 D. 若x=4,每生成1molS,转移的电子为6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学欲在实验室中用乙醇制备1,2-二溴乙烷。
甲同学设计的实验装置如下图:
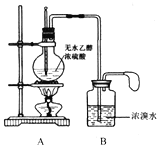
(1)请写出A和B中发生的主要反应的化学方程式
A:________________________________________。
B:________________________________________。
(2)乙同学查阅资料得知:
①此反应可能存在的主要副反应有:在浓硫酸的存在下,乙醇可发生如下反应生成乙醚, ![]()
②乙醚不与溴水反应
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
颜色、状态 | 无色液体 | 无色液体 | 无色液体 |
沸点/℃ | 78.5 | 132 | 34.6 |
若最终产物中混有少量乙醚,可用__________的方法除去。
(3)丙同学观察到:在实验后期A中液体变黑,认为应该在装置A和B之间加入装置__________(填序号),此装置的作用是____________________。
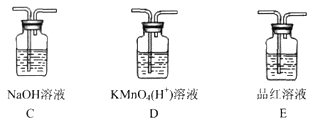
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含MgCl2和AlCl3各0.01 mol,向其中逐滴滴加1 mol/L的NaOH溶液至过量,下列关系图正确的是( )


A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气代替石油生产液体燃料和基础化学品是当前化学研究和发展的重点。
(1)我国科学家创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产乙烯、芳香烃Y和芳香烃Z等重要化工原料,实现了CO2的零排放,碳原子利用率达100%。已知Y、Z的相对分子质量分别为78、128,其一氯代物分别有1种和2种。
①有关化学键键能数据如表中所示:
化学键 | H-H | C=C | C-C | C≡C | C-H |
E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
写出甲烷一步生成乙烯的热化学方程式:_________________________,反应中硅化物晶格限域的单中心铁催化剂的作用是________________________;
②已知:原子利用率=期望产物总质量/反应物总质量×100%,则甲烷生成芳香烃Y的原子利用率为___________;
③生成1 mol Z产生的H2约合标准状况下________L。
(2)如图为乙烯气相直接水合法制备乙醇过程中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
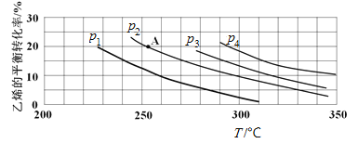
①若p2=8.0 MPa,列式计算A点的平衡常数Kp=____________(用平衡分压代替平衡浓度计算;分压=总压×物质的量分数;结果保留到小数点后两位);
②该反应为__________(填“吸热”或“放热”)反应,图中压强(p1、p2、p3、p4)的大小关系为____________,理由是________________;
③气相直接水合法常采用的工艺条件:磷酸/硅藻土为催化剂,反应温度为290℃,压强为6.9 MPa,n(H2O)∶n(C2H4)=0.6∶1。乙烯的转化率为5%,若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有______________(任写两条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,改变反应物用量或浓度,不会改变反应产物的是( )
A. 铁在硫蒸气中燃烧 B. SO2通入石灰水
C. 氯气通入KI溶液 D. H2SO4中加入铁粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com