
已知化学反应2C(s)+O2(g) 2CO(g);2CO(g) + O2(g)
2CO(g);2CO(g) + O2(g)  2CO2(g)都是放热反应。据此推断,下列说法不正确的是(相同条件下)
2CO2(g)都是放热反应。据此推断,下列说法不正确的是(相同条件下)
A.56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量
B.28gCO所具有的能量一定高于12gC所具有的能量
C.12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D.将两份等质量碳燃烧,生成CO2的反应比生成CO的反应放出的热量多
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年吉林省高一入学摸底考试化学试卷(解析版) 题型:选择题
将点燃的火柴竖直向上,火柴不易继续燃烧,其原因是( )
A.火柴梗温度达不到着火点 B.火柴梗的着火点比火柴头的高
C.火柴梗潮湿,不易继续燃烧 D.火柴梗接触氧气少
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
0.5molNa2SO4中所含Na+的数目为( )
A.3.02×1023 B.6.02×1023 C.0.5 D. 1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
有关碰撞理论,下列说法中不正确的是
A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应
B.增大反应物浓度,单位体积内活化分子数增多,有效碰撞几率增大,反应速率增大
C.升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大
D.正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
101KPa ② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是
A.碳的燃烧热等于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.CH4(g) + 3/2O2(g) == CO(g) +2H2O(l) ΔH== -a kJ·mol—1 ,这里ΔH代表燃烧热
B.在250C、101kPa,1mol硫和2mol硫的燃烧热相等
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应
D.101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:填空题
某烧杯中盛有100 mL FeCl3和CuCl2的混合液,混合溶液中c(FeCl3)=1 mol/L,
c(CuCl2)=1 mol/L。请回答:
(1)该混合溶液中铁离子的物质的量为 ;铜离子的物质的量为 ;
(2)该混合溶液中氯离子的物质的量n(Cl-)= ;
(3)该混合溶液中氯离子的物质的量浓度c(Cl-)= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
在实验室里进行分液操作,下列实验仪器中一定需要使用的是
A.容量瓶 B.分液漏斗 C.玻璃棒 D.温度计
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:填空题
(8分)氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。氯碱工业中制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。学校实验小组精制粗盐水的实验过程如下:
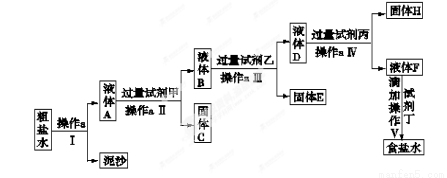
请回答以下问题:
(1)操作a的名称是 ,所用玻璃仪器是 。
(2)在第Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为 溶液。
(3)判断加入试剂乙已过量的方法是 。
(4)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com