
如图是制取乙酸乙酯的装置,下列说法中错误的是( )。
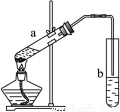
A.浓硫酸在此反应中作为催化剂、吸水剂
B.b中导气管不能插入饱和碳酸钠溶液中,目的是防止倒吸
C.试管a中加入碎瓷片目的是防止剧烈沸腾
D.先向试管a中加入浓硫酸,然后依次加入酒精、乙酸
科目:高中化学 来源: 题型:阅读理解
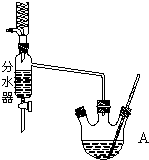 如图为制取乙酸乙酯的实验装置图.回答下列问题:
如图为制取乙酸乙酯的实验装置图.回答下列问题:| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
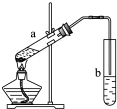
| A、浓硫酸在此反应中作为催化剂、吸水剂 | B、b中导气管不能插入饱和碳酸钠溶液中,目的是防止倒吸 | C、试管a中加入碎瓷片目的是防止剧烈沸腾 | D、先向试管a中加入浓硫酸,然后依次加入酒精、乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
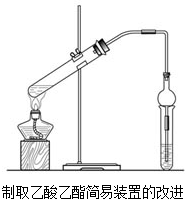 现用如图装置制取乙酸乙酯.请回答:
现用如图装置制取乙酸乙酯.请回答:查看答案和解析>>
科目:高中化学 来源:2009届上海市南汇中学高三年级零次月考、化学试卷 题型:058
乙酸乙酯是重要的工业原料和溶剂.现利用如图装置制取乙酸乙酯的粗产品,再测定乙酸乙酯的含量.

(1)写出反应方程式________(反应)
(2)实验室一般用饱和碳酸钠溶液接收反应的生成物.若不振荡该试管,可看到的现象是________,若振荡该试管,可看到的现象是________,但是有却出现了白色晶体,该晶体是________;
(3)对于制乙酸乙酯的上述装置,为了提高产率,请提出一条改进意见:
________.
(4)为测定乙酸乙酯的含量,进行如下操作:
(Ⅰ)准确称量20.0 g乙酯乙酯粗品于锥形瓶中,用0.50 mol/L NaOH滴定(酚酞做示剂).终点时消耗NaOH溶液的体积为40.0 mL
(Ⅱ)另取20.0 g乙酸乙酸粗产品于250 mL锥形瓶中,加入100 mL的2.1 mol/L NaOH溶液混合增色匀后,装上冷凝管,在水浴上加热回流约1小时,装置如图所示.待冷却后,用0.50 mol/LHC1滴定过量的NaOH.终点时消耗盐酸的体积为20.0 mL.
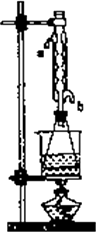
回答:①实验(Ⅰ)中达到滴定终点时的现象是________.
②实验(Ⅱ)中冷水从冷水凝管的________(填a或b)管口通入.
③利用实验(Ⅰ)、(Ⅱ)测量的数据计算粗产物中乙酸乙酯的质量分数为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com