
�����ǵ�ѭ���е���Ҫ���ʣ�����������������������Ź㷺��Ӧ�á�
��1����ͼ��N2��H2��Ӧ�����������仯��ʾ��ͼ����÷�Ӧ����Һ̬�����Ȼ�ѧ����ʽ�� ��
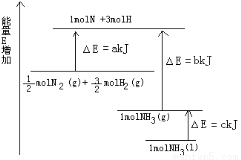
��2����֪����H2O(g)=H2O(l) ��H����Q1 kJ��mol��1
��C2H5OH(g)��3O2(g)=2CO2(g)��3H2O(g) ��H����Q2 kJ/mol ��C2H5OH(g)=C2H5OH(l) ��H����Q3 kJ/mol
��23 gҺ��ƾ���ȫȼ������CO2(g)��H2O(l)���ͷų�������Ϊ kJ������Q1��Q2��Q3����ʾ ��
��1��N2(g) +3H2(g)  2NH3(l) ��H= -2(b+c-a) kJ/mol��2��(0.5Q2��1.5Q1��Q3)
2NH3(l) ��H= -2(b+c-a) kJ/mol��2��(0.5Q2��1.5Q1��Q3)
��������
���������(1)����ͼʾ��֪���ɷ�Ӧ���������������������Ĺ�ϵ��֪N2��H2��Ӧ����Һ̬�����Ȼ�ѧ����ʽ��N2(g) +3H2(g)  2NH3(l) ��H= -2(b+c-a) kJ/mol����2���ڣ��ۣ�3���������ɵ�C2H5OH(g)+ 3O2(g)=2CO2(g)��3H2O(l) ��H=��(Q2+3Q1��Q3) kJ/mol��1mol���Ҵ�����Ϊ46g.����23 gҺ��ƾ���0.5mol��ȫȼ������CO2(g)��H2O(l)���ͷų�������Ϊ(0.5Q2��1.5Q1��Q3)KJ.
2NH3(l) ��H= -2(b+c-a) kJ/mol����2���ڣ��ۣ�3���������ɵ�C2H5OH(g)+ 3O2(g)=2CO2(g)��3H2O(l) ��H=��(Q2+3Q1��Q3) kJ/mol��1mol���Ҵ�����Ϊ46g.����23 gҺ��ƾ���0.5mol��ȫȼ������CO2(g)��H2O(l)���ͷų�������Ϊ(0.5Q2��1.5Q1��Q3)KJ.
���㣺�����Ȼ�ѧ����ʽ����д����Ӧ�ȵļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡͬ����ʱ�����˽�ѡ��4��1.2 ȼ������Դ�Ծ��������棩 ���ͣ�ѡ����
���и������ʵ�ȼ������ȵ���(����)
A��̼��һ����̼B��1 mol̼��2 mol̼ C��3 mol��ϩ�ͱ� D�����ۺ���ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��2.3��ѧƽ���ƶ��Ծ��������棩 ���ͣ�ѡ����
�Դ���ƽ��״̬�ķ�Ӧ��2A(g)+B(g)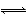 2C(g)(��֪��ӦΪ���ȷ�Ӧ)������������ȷ����(����)
2C(g)(��֪��ӦΪ���ȷ�Ӧ)������������ȷ����(����)
A������ѹǿ��v(��)����v(��)��С
B�������¶ȣ�v(��)��С��v(��)����
C������AŨ�ȵ�˲�䣬v(��)����v(��)����
D������AŨ�ȵ�˲�䣬v(��)�����v(��)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��1.3��ѧ��Ӧ�ȵļ��㣨�����棩 ���ͣ������
���ྻú�������о����������൱�ձ飬������Աͨ����ú����¯�н�����������ˮ�����ķ�����������������ֵ�ߴ�12 500~16 000 kJ��m-3��ú̿��������Ҫ�ɷ���CO��H2��CO��H2����Ϊ��Դ�ͻ���ԭ�ϣ�Ӧ��ʮ�ֹ㷺����֪��
C(s)+O2(g) CO2(g)����H1=-393��5 kJ��mol-1��
CO2(g)����H1=-393��5 kJ��mol-1��
2H2(g)+O2(g) 2H2O(g)����H2=-483��6 kJ��mol-1��
2H2O(g)����H2=-483��6 kJ��mol-1��
C(s)+H2O(g) CO(g)+H2(g)����H3=+131��3 kJ��mol-1��
CO(g)+H2(g)����H3=+131��3 kJ��mol-1��
��ӦCO(g)+H2(g)+O2(g) H2O(g)+CO2(g)����H=�������� kJ��mol-1����״���µ�ú̿��(CO��H2)33��6 L��������ȫ��Ӧ����CO2��H2O����Ӧ������ת�ơ������� mol e-��
H2O(g)+CO2(g)����H=�������� kJ��mol-1����״���µ�ú̿��(CO��H2)33��6 L��������ȫ��Ӧ����CO2��H2O����Ӧ������ת�ơ������� mol e-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��1.3��ѧ��Ӧ�ȵļ��㣨�����棩 ���ͣ�ѡ����
��֪3��6 g̼��6��4 g��������ȼ�գ�����Ӧ��ľ����ų�X kJ��������֪����̼ȼ���ȵĦ�HΪ-Y kJ�� mol-1����1 mol C��O2��Ӧ����CO�ķ�Ӧ�Ȧ�HΪ(����)
A��-(5X-0��5Y) kJ�� mol-1
B��-Y kJ�� mol-1
C��-(10X-Y) kJ�� mol-1
D��+(10X-Y) kJ�� mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£���һ�ݻ�������ܱ������У���ӦA(g) + 2B (g)  3C(g)��ƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ3 mol��2 mol��4 mol�����¶Ȳ��䣬�������ڵ�ƽ���������ټ���A��C��1mol����ʱ��ƽ���ƶ��ķ�����( )
3C(g)��ƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ3 mol��2 mol��4 mol�����¶Ȳ��䣬�������ڵ�ƽ���������ټ���A��C��1mol����ʱ��ƽ���ƶ��ķ�����( )
A�������ƶ� B�������ƶ� C�����ƶ� D�����ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£���Һ������Զ�TiO2���Ⱦ��R���ⷴӦ��Ӱ����ͼ��ʾ�������ж���ȷ����( )

A����0-50 min֮�䣬 pH = 2��PH = 7ʱR�Ľ���ٷ��ʲ����
B���� 20-25 min֮�䣬 pH = 10 ʱR��ƽ����������Ϊ0.04 mol?L-1?min-1
C����Һ����Խǿ�� R �Ľ�������ԽС
D��R����ʼŨ�Ⱥ���Һ��PH��Ӱ��R�Ľ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ĸ�����ѧ�ڵ�һ���¿������Ծ��������棩 ���ͣ�ѡ����
����ʵ���ܴﵽĿ�ĵ���
A��ֻ�μӰ�ˮ����NaCl��AlCl3��MgCl2��Na2SO4������Һ
B����NH4Cl��Һ�����Ʊ�NH4Cl����
C������ȡ��Һ�ķ�����ȥ�ƾ��е�ˮ
D���ÿɼ�����������������Һ�ͽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���Ĵ�ʡ�ɶ���2012������Ի�ѧ�Ծ��������棩 ���ͣ������
��9�֣�����ʯ����Ҫ�ɷ���K2SO4��Al2(SO4)3��2Al2O3��6H2O��������������
��������ʯ�Ʊ�K2SO4�Ĺ�������������ʾ��
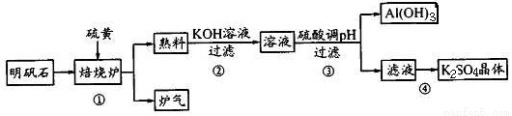
��1������¯�з������·�Ӧ�����ڷ���ʽ�б�ʾ������ת�Ƶķ������Ŀ
2Al2(SO4)3��3S 2Al2O3��9SO2��
2Al2O3��9SO2��
��2��������漰Al2O3�����ӷ���ʽΪ____��
��3������۵�pH����AI{OH)�������ӷ���ʽΪ____��������CO2����pH��������
.
��4������ܵ���Ҫ����������___ _�����ˡ�ϴ�Ӻ���
��5��¯�����տ���������;�����һ����__ _��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com