

分析 (1)空气中的CO2属于酸性氧化物,能溶于强碱溶液;
(2)①根据图知,碱性条件下H3AsO3的浓度减小、H2AsO3-浓度增大,说明碱和H3AsO3生成H2AsO3-,该反应为酸碱的中和反应;
②Ka1=$\frac{c({H}_{2}As{{O}_{4}}^{-}).c({H}^{+})}{c({H}_{3}As{O}_{4})}$,pH=2.2时c(H+)=10-2.2 mol/L,c(H3AsO3)=c(H2AsO3-);
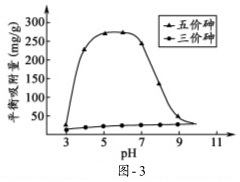
(3)①吸附剂X表面所带负电荷增多,静电斥力越大;
②在pH4~7之间,吸附剂X表面带正电,五价砷主要以H2AsO4-和HAsO42-阴离子存在,pH<7.1时带正电荷,pH越低,表面所带正电荷越多;而三价砷主要以H3AsO3分子存在;
在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,如果能将三价砷转化为五价砷,能有效的去除三价砷.
解答 解:(1)空气中的CO2属于酸性氧化物,能溶于强碱溶液,NaOH是碱,能吸收空气中的二氧化碳而生成碳酸根离子,所以其原因是碱性溶液吸收了空气中的CO2,故答案为:碱性溶液吸收了空气中的CO2;
(2)①根据图知,碱性条件下H3AsO3的浓度减小、H2AsO3-浓度增大,说明碱和H3AsO3生成H2AsO3-,该反应为酸碱的中和反应,同时还生成水,离子方程式为OH-+H3AsO3=H2AsO3-+H2O,
故答案为:OH-+H3AsO3=H2AsO3-+H2O;
②Ka1=$\frac{c({H}_{2}As{{O}_{4}}^{-}).c({H}^{+})}{c({H}_{3}As{O}_{4})}$,pH=2.2时c(H+)=10-2.2 mol/L,c(H3AsO3)=c(H2AsO3-),p Ka1=-lg Ka1=-lg$\frac{c({H}_{2}As{{O}_{4}}^{-}).c({H}^{+})}{c({H}_{3}As{O}_{4})}$=2.2,
故答案为:2.2;
(3)①吸附剂X表面所带负电荷增多,静电斥力越大,在pH7~9之间,随pH升高H2AsO4-转变为HAsO42-,吸附剂X表面所带负电荷增多,静电斥力增加,导致在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,
故答案为:在pH7~9之间,随pH升高H2AsO4-转变为HAsO42-,吸附剂X表面所带负电荷增多,静电斥力增加;
②在pH4~7之间,吸附剂X表面带正电,五价砷主要以H2AsO4-和HAsO42-阴离子存在,pH<7.1时带正电荷,pH越低,表面所带正电荷越多,所以静电引力较大;而三价砷主要以H3AsO3分子存在,与吸附剂X表面产生的静电引力小,所以在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱;
在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,如果能将三价砷转化为五价砷,能有效的去除三价砷,所以采取的措施是加入氧化剂,将三价砷转化为五价砷,
故答案为:在pH4~7之间,吸附剂X表面带正电,五价砷主要以H2AsO4-和HAsO42-阴离子存在,静电引力较大;而三价砷主要以H3AsO3分子存在,与吸附剂X表面产生的静电引力小;加入氧化剂,将三价砷转化为五价砷.
点评 本题以含有As的物质为载体考查弱电解质的电离及图象分析,为高频考点,侧重考查学生对基础知识的掌握和灵活运用、图象分析判断能力,明确出题人的目的是解本题关键,难点是图象的正确理解和分析,题目难度中等.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
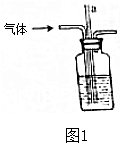 某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2
某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .B→C的反应条件为加热(或煅烧),C→Al的制备方法称为电解法.
.B→C的反应条件为加热(或煅烧),C→Al的制备方法称为电解法.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe$→_{点燃}^{Cl_{2}}$FeCl2$\stackrel{NaOH(ap)}{→}$Fe(OH)2 | |
| B. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | CaCO3$\stackrel{高温}{→}$CaO$→_{高温}^{SiO_{2}}$CaSiO3 | |
| D. | NH3$→_{催化剂、△}^{O_{2}}$NO$\stackrel{H_{2}O}{→}$HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v生成(CH3OH)=v消耗(CO) | |
| B. | 混合气体的密度不再改变 | |
| C. | 混合气体的平均相对分子质量不再改变 | |
| D. | CO、H2、CH3OH的浓度比为1:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将乙烯通入酸性KMnO4溶液中 | 证明乙烯能发生加成反应 |
| B | 向含酚酞的NaOH溶液中加入氯水 | 证明Cl2具有漂白性 |
| C | 常温下,向Fe和Cu中分别加入稀盐酸 | 比较Fe和Cu的金属活动性 |
| D | 将两根铁钉分别放入甲乙两支试管中,甲为干燥的试管,乙中含有少量食盐水. | 证明有NaCl参加反应,腐蚀速率更快 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器编号 | 物质的起始浓度(mol•L-1) | 物质的平衡浓度(mol•L-1) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
| A. | 达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为 4:5 | |
| B. | 达平衡时,容器Ⅱ中 c(O2 )/c(NO2 ) 比容器Ⅰ中的大 | |
| C. | 达平衡时,容器Ⅲ中 NO 的体积分数小于50% | |
| D. | 当温度改变为 T2时,若 k正=k逆,则 T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
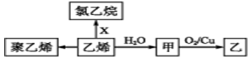
| A. | 甲与CH3OCH3互为同分异构体 | B. | X为Cl2 | ||
| C. | 聚乙烯是纯净物 | D. | 甲→乙反应类型为取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com