
A、图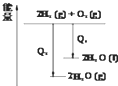 表示氢气与氧气反应中的能量变化 表示氢气与氧气反应中的能量变化 | B、图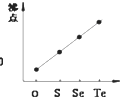 表示气态氢化物沸点 表示气态氢化物沸点 | C、图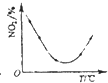 表示在容积相同的恒容密闭容器中,等量的NO2在不同温度下反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 表示在容积相同的恒容密闭容器中,等量的NO2在不同温度下反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | D、图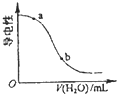 表示CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b 表示CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、图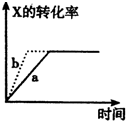 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 | B、图 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 | C、图 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 | D、图 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com