
���� ��1�����������������ʹFe2+����ΪFe3+�����������µ����ʣ���������ҺpH=4��ʹFe3+ת��ΪFe��OH��3�����Դﵽ��ȥFe3+������ʧCuSO4��Ŀ�ģ���Ӻ�ͭԪ�ص������������ӷ�Ӧ�ٽ�������ˮ��ת��Ϊ������
��2����Ksp[Mg��OH��2]=1.8��10-11��Ksp[Cu��OH��2]=2.2��10-20��֪��������ͭ�����ܣ������ɣ�
��3�������ֳ�������ʱ����Һ��AgCl��AgBr�ı�����Һ����Һ��$\frac{c��B{r}^{-}��}{c��C{l}^{-}��}$=$\frac{Ksp��AgBr��}{Ksp��AgCl��}$���Դ������
��4�����ݳ���ת����ԭ����������Ӧ������ܵķ�����У�
��� �⣺��1���ټ��������������ʹFe2+����ΪFe3+�����������µ����ʣ�A��C��D�л��������ʣ�ֻ�й�������Ļ�ԭ����Ϊˮ�����������ʣ���ֻ��B���ϣ��ʴ�Ϊ��B��
�ڵ�������ҺpH=4��ʹFe3+ת��ΪFe��OH��3�����Դﵽ��ȥFe3+������ʧCuSO4��Ŀ�ģ���Ӻ�ͭԪ�ص������������ӷ�Ӧ�ٽ�������ˮ��ת��Ϊ��������C��D���ɣ�A��B��ͭ����ת��Ϊ�����������ϣ�
�ʴ�Ϊ��CD��
��2�����ܵ���ʵ��ܶȻ�ԽС�����백ˮʱԽ�����ɳ����������ɵij���ΪCu��OH��2����Ӧ�����ӷ���ʽΪCu2++2NH3•H2O=Cu��OH��2��+2NH4+��
�ʴ�Ϊ��Cu��OH��2��Cu2++2NH3•H2O=Cu��OH��2��+2NH4+��
��3�������ֳ�������ʱ����Һ��AgCl��AgBr�ı�����Һ����Һ��$\frac{c��B{r}^{-}��}{c��C{l}^{-}��}$=$\frac{Ksp��AgBr��}{Ksp��AgCl��}$=$\frac{5.4��1{0}^{-13}}{2.0��1{0}^{-10}}$=2.7��10-3��
�ʴ�Ϊ��2.7��10-3��
��4����ʢ��1mL 0.1mol/L MgCl2��Һ���Թ��еμ�2��2mol/L NaOH��Һ���а�ɫ�������ɣ��ٵμ�2��0.1mol/LFeCl3��Һ�����ã����Թ۲쵽��ɫ����ת��Ϊ���ɫ������˵�����������ܽ��С��������þ������ת�������ӷ���ʽ��2Fe3++3Mg��OH��2=2Fe��OH��3+3Mg2+��
�ʴ�Ϊ����ɫ����ת��Ϊ���ɫ������2Fe3++3Mg��OH��2=2Fe��OH��3+3Mg2+��
���� ���⿼����������ᴿ�����ܵ���ʵ��ܽ�ƽ�⣬Ϊ��Ƶ���㣬�������ʵ����ʡ����ʲ��켰�ܽ�ƽ��ļ����Ϊ���Ĺؼ������ػ��������ᴿ����������������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe+2HCl�TFeCl2+H2�� | |
| B�� | 2HCl+Ca��ClO��2�T2HClO+CaCl2 | |
| C�� | I2+2NaClO3�T2NaIO3+Cl2�� | |
| D�� | 4HCl��Ũ��+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ����� | ʵ������ | ʵ���� |
| 1 | ��AgNO3��Һ | �а�ɫ�������� |
| 2 | ������NaOH��Һ������ | �ռ�������1.12L��������ɱ�״���µ������ |
| 3 | ������BaCl2��Һ����Ӧ����й��ˡ�ϴ�ӡ������������������м�����ϡ���ᣬȻ�������� | ��һ�γ�������Ϊ6.27g���ڶ��γ�������Ϊ2.33g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
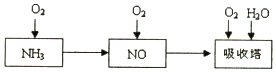
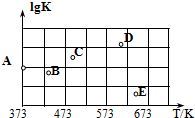 �Ȼ���������ҽҩ��ũҩ��Ⱦ�Ϲ�ҵ���л��ϳɹ�ҵ�������Ȼ���������Ȼ�������Li/SOCl2����أ���ҵ����SO2��SCl2��Cl2��Ӧ�ϳ�SO2��g��+Cl2��g��+SCl2��g��?2SOCl2��g����
�Ȼ���������ҽҩ��ũҩ��Ⱦ�Ϲ�ҵ���л��ϳɹ�ҵ�������Ȼ���������Ȼ�������Li/SOCl2����أ���ҵ����SO2��SCl2��Cl2��Ӧ�ϳ�SO2��g��+Cl2��g��+SCl2��g��?2SOCl2��g����| t/min | 0 | 1 | 2 | 3 | 4 | 5 | |
| I | p | 6.0p0 | 6.7p0 | 6.1p0 | 5.4p0 | 5.0p0 | 5.0p0 |
| II | p | 6.0p0 | 7.0p0 | 5.3p0 | 5.0p0 | 5.0p0 | 5.0p0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com