
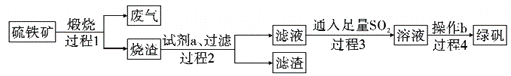
【题目】由硫铁矿(主要成分:FeS2和SiO2)为主要原料得到绿矾(FeSO4·7H2O)的流程如下:
下列说法不正确的是( )
A. 过程1,废气中含SO2
B. 过程2,试剂a为稀硫酸
C. 过程3,离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
D. 过程4,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
【答案】D
【解析】由制备绿矾流程可知,硫铁矿(主要成分:FeS2和SiO2)高温煅烧后的烧渣(主要成分:Fe2O3和SiO2)溶于硫酸,溶液中含Fe3+,过程2过滤除去二氧化硅,滤液中通入二氧化硫,将铁离子还原生成亚铁离子,过程4为蒸发浓缩、冷却结晶析出绿矾。A.根据上述分析,过程1,废气中含SO2,故A正确;B.因绿矾的酸根离子为硫酸根离子,则过程2最好用硫酸来溶解烧渣,故B正确;C. 过程3中二氧化硫将铁离子还原生成硫酸亚铁,离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故C正确;D. 过程4,将溶液加热到有较多固体析出,再用余热将液体蒸干,蒸干时绿矾受热失去结晶水,得不到纯净绿矾,故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-) 、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )
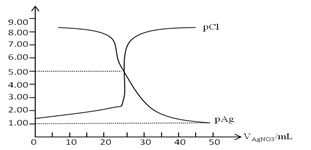
A. AgCl的沉淀溶解平衡常数Ksp数量级为10-10
B. 为防止指示剂失效,溶液应维持中性或弱碱性
C. 滴定中指示剂的有效浓度应维持在2.0×10-2 mol/L
D. 滴定完后加入1mL 0.01mol/L H2SO4会产生新的沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:
(1)Ⅱ中含氧官能团的名称 .
(2)反应②的化学方程式 .
(3)下列说法正确的是 .
A.Ⅰ和Ⅴ均属于芳香烃
B.Ⅱ能发生银镜反应
C.Ⅱ能与4molH2发生加成反应
D.反应③属于酯化反应
(4)A的结构简式 .
(5)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种.写出满足上述条件的Ⅵ的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】m g铝镁合金与一定浓度的稀硝酸恰好完全反应(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加a mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n g,则下列有关该实验的说法中错误的是( )
A. 沉淀中OH-的质量为(n-m)g
B. 恰好溶解后溶液中的NO的物质的量为aVmol
C. 反应过程中转移的电子的物质的量为![]() mol
mol
D. 与合金反应的硝酸的物质的量为(![]() +
+![]() )mol
)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中的成盐元素除了氯之外,还有溴和碘。
(1)工业上可用Cl2和NH4Cl溶液反应制取NCl3(NCl3既可用于漂白,又可用于柠檬等水果的熏蒸处理)。当用干燥洁净的玻璃棒蘸取NCl3滴到干燥的红色石蕊试纸上,试纸不褪色;若取NCl3滴入50-60oC热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,则试纸先变蓝后褪色。写出对应该现象的化学方程式:____________________________________________________。
(2)①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:______KIO3+ ______KI + H2SO4 = ______K2SO4+_____I2+ ______
②上述反应生成的I2可用四氯化碳检验,现象为________________________________________。
(3)NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
粒子 | I2 | Br2 | IO3- |
物质的量物的/mol | 0.5 | 1.3 | x |
则x= ______;原溶液中NaI的物质的量为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,向50mL 0.018mol/L AgNO3溶液中加入50mL 0.02mol/L 盐酸生成沉淀.已知:Ksp(AgCl)=1.8×10﹣10 , 则生成沉淀后的体系中c(Ag+)为( )
A.1.8×10﹣7mol/L
B.1.8×10﹣8 mol/L
C.1.8×10﹣9mol/L
D.1.8×10﹣10mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2氯丙烷制取少量的1,2丙二醇经过下列哪几步反应( )
A. 加成→消去→取代 B. 消去→加成→水解
C. 取代→消去→加成 D. 消去→水解→加成消
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定浓度的下列溶液,不外加任何试剂就能依次鉴别出来,正确的鉴别顺序为( ) ①NaOH溶液②(NH4)2SO4溶液③BaCl2溶液④KNO3溶液⑤FeCl3溶液.
A.①②③④⑤
B.②③⑤④①
C.⑤①②③④
D.⑤③②①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com