
| �¶�/�� | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
| c(CO) |
| c(CO2) |
| x |
| 4-x |
| 2 |
| 4 |
| 2mol/2L |
| 5min |
| c(CO) |
| c(CO2) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ȼ�ͭ��Һʱ������ |
| B��ͭ��ԭ��صĸ�����������ҺΪ����ʣ� |
| C�����ʳ��ˮʱ������ |
| D����Ƭ�϶�пʱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2 |
| B��CO2 |
| C������ |
| D��O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
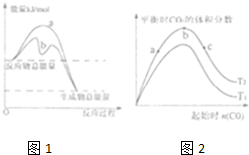 ��ҵ���о�ȼ������Ĺ����У��漰���·�Ӧ��
��ҵ���о�ȼ������Ĺ����У��漰���·�Ӧ��| 1 |
| 2 |
| 1 |
| 2 |
| t/s | 0 | 50 | 100 | 150 | 200 |
| C��CO��/mol��L- | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ϳɹ��ˣ���ͨѶ����� |
| B���ϳ�ҩ������������ |
| C������Ϳ�ϣ��û������˾� |
| D����ϩ���У����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ᣬ�������ƣ�̼���ƣ������� |
| B�����ᣬ�������ƣ���̪������ͭ |
| C���������ƣ�����þ��̼���ƣ������� |
| D���Ȼ����������ƣ��Ȼ��ƣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��150 mL |
| B��200 mL |
| C��450 mL |
| D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ����ͭ |
| B��CuSO4?5H2O |
| C��Ũ���� |
| D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ɷ� | NaOH | Na2CO3 | H2O |
| �������� | 90.4% | 3.8% | 5.8% |
| A��4.68 g |
| B��5.85 g |
| C��2.34 g |
| D����2.34-a�� g |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com