
| A. | 反应(1)和(2)均为氧化还原反应 | |
| B. | 反应(1)的氧化剂是O2,还原剂是FeO•Cr2O3 | |
| C. | 高温下,O2的氧化性大于Fe2O3小于Na2CrO4 | |
| D. | 生成1mol的Na2Cr2O7时共转移5mol电子 |
分析 A、化学反应中有元素化合价变化的反应是氧化还原反应,没有化合价变化的化学反应不是氧化还原反应;
B、得电子化合价降低的物质是氧化剂,失电子化合价升高的物质是还原剂;
C、同一化学反应中氧化剂的氧化性大于氧化产物的氧化性;
D、反应只有O元素的化合价降低,由0价降低为-2价,电子转移的物质的量为参加反应的氧气的物质的量的4倍,由方程式可知计算Na2CrO4与转移电子数,再换算为生成1mol的Na2Cr2O7时转移电子数.
解答 解:A、4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2中有元素化合价的变化,所以是氧化还原反应,而2Na2CrO4+H2SO4$\frac{\underline{\;高温\;}}{\;}$Na2SO4+Na2Cr2O7+H2O中没有元素化合价的变化,所以不是氧化还原反应,故A错误;
B、4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2中,氧气中氧元素得电子化合价降低,所以氧化剂是氧气,铁元素和铬元素失电子化合价升高,所以还原剂是FeO•Cr2O3,故B正确;
C、4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2中,氧化剂是氧气,还原剂是FeO•Cr2O3,所以氧气的氧化性大于Na2CrO4和Fe2O3,但不能判断Na2CrO4和Fe2O3的氧化性相对强弱,故C错误;
D、由方程式4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2转移电子可知,生成1molNa2CrO4时,参加反应的O2的物质的量为$\frac{7}{8}$mol,反应中O元素由0价降低为-2价,电子转移的物质的量为参加反应的氧气的物质的量的4倍,转移电子的物质的量为$\frac{7}{8}$mol×4=3.5mol,所以反应(1)中每生成1molNa2CrO4时电子转移3.5mol,反应(2)不是氧化还原反应,所以生成1mol的Na2Cr2O7时转移7mol电子,故D错误;
故选B.
点评 本题考查了氧化剂和还原剂的判断、氧化还原反应的判断等知识点,根据元素化合价的变化判断氧化还原反应、氧化剂和还原剂即可分析解答本题.


科目:高中化学 来源: 题型:选择题
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、H+、SO32-、NO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
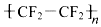 )的材料.
)的材料.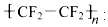 是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )| A. | CF2=CF2能使溴的CCl4溶液褪色 | |
| B. | 四氟乙烯合成聚四氟乙烯属于加聚反应 | |
| C. | 1molCF2=CF2只能与1molH2发生加成反应 | |
| D. | 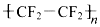 能使高锰酸钾酸性溶液褪色 能使高锰酸钾酸性溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓的强酸和稀的强碱反应 | B. | 浓的弱酸和稀的强碱反应 | ||
| C. | 等浓度的强酸和弱碱反应 | D. | 二元强酸与一元强碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硫酸转移至容量瓶中,加水稀释至距标线2~3 cm处,改用胶头滴管定容 | |
| B. | 用酒精萃取碘水中的碘单质 | |
| C. | 进行液体蒸馏实验时,冷凝管中应充满自来水 | |
| D. | 某溶液加入盐酸酸化的氯化钡溶液后,出现白色沉淀,则原溶液中必有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>②>① | B. | ②>③>① | C. | ①>②>③ | D. | ③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 | B. | 50 | C. | 5×l03 | D. | 104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当x≤n时,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 当x≥$\frac{3n}{2}$时,反应的离子方程式为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| C. | 当n≤x≤$\frac{3n}{2}$时,反应中转移电子的物质的量n(e-)为2nmol≤n(e-)≤3nmol | |
| D. | 当n<x<$\frac{3n}{2}$时,溶液中Fe3+、Cl-、I2的物质的量之比为2(x-n):x:n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COO-)>c(Ba2+)>c(OH-)>c(H+) | B. | c(H+)+c(Ba2+)=c(CH3COO-)+c(OH-) | ||
| C. | c(OH-)═c(H+)+c(CH3COO-) | D. | 2c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com