
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案科目:高中化学 来源:不详 题型:单选题
 Fe+TiO2+H2O,下列有关该反应的说法错误的是( )
Fe+TiO2+H2O,下列有关该反应的说法错误的是( )| A.FeTiO3中Fe显+2价,Ti显+4价 | B.TiO2既不是氧化产物也不是还原产物 |
| C.反应中生成1 mol铁将转移3 mol电子 | D.FeTiO3在反应中作氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
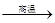 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2 +8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。
+8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。 2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。
2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2d+3f=3g+h | B.反应中每消耗5.6gFe,转移0.2mol~0.3mole- |
| C.HNO3的氧化性大于Fe3+ | D.当a不变时,d随着b的增大而增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.被氧化的元素是Cu和S |
| B.MnO4-是氧化剂,Cu2S既是氧化剂又是还原剂 |
| C.氧化剂与还原剂的物质的量之比为8∶5 |
| D.生成2.24 L(标况下) SO2,转移电子的物质的量是0.8 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Na2CO3 | B.KMnO4 | C.XeO3 | D.Na2SO3 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com