
��12�֣�CoCl2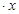 H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2
H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2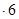 H2O��һ���¹�����������ͼ��
H2O��һ���¹�����������ͼ�� 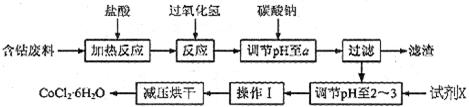
��֪��
���������ᷴӦ�Ļ�ѧ����ʽΪ��Co+2HCl=CoCl2+H2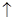
��CoCl2��6H2O�۵�86�棬������ˮ�����ѵȣ��������ȶ�����������110~120��ʱ��ʧȥ�ᾧˮ����ж�����ˮ�Ȼ��ܡ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
| ������ | 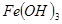 | 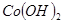 | 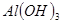 |
| ��ʼ���� | 2.3 | 7.6 | 3.4 |
| ��ȫ���� | 4.1 | 9.2 | 5.2 |
 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�






| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��12�֣�CoCl2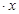 H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2
H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2 H2O��һ���¹�����������ͼ��
H2O��һ���¹�����������ͼ��

��֪��
���������ᷴӦ�Ļ�ѧ����ʽΪ��Co+2HCl=CoCl2+H2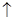
��CoCl2��6H2O�۵�86�棬������ˮ�����ѵȣ��������ȶ�����������110~120��ʱ��ʧȥ�ᾧˮ����ж�����ˮ�Ȼ��ܡ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
|
������ |
|
|
|
|
��ʼ���� |
2.3 |
7.6 |
3.4 |
|
��ȫ���� |
4.1 |
9.2 |
5.2 |
��ش��������⣺
��1��д�������������ʱ��Һ�з��������ӷ�Ӧ����ʽ��__________
��2������̼���Ƶ���pH��a��a�ķ�Χ��__________��
��3������ʵ��Լ�X��__________
��4������I����3������ʵ�������������__________��__________�ͼ�ѹ���ˡ�
��5���Ƶõ�CoCl2��6H2O���ѹ��ɵ�ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
CoCl2![]() H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2
H2O�ڼ���ʱ����ʧˮ�������ֲ�ͬ����ɫ��ʵ����������Ƴɱ�ɫ�轺�����Ը��ﲢ��֤ˮ�ݡ��Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2![]() H2O��һ���¹�����������ͼ��
H2O��һ���¹�����������ͼ��
��֪��
���������ᷴӦ�Ļ�ѧ����ʽΪ��Co+2HCl=CoCl2+H2![]()
��CoCl2·6H2O�۵�86�棬������ˮ�����ѵȣ��������ȶ�����������110~120��ʱ��ʧȥ�ᾧˮ����ж�����ˮ�Ȼ��ܡ�
�۲���������������������ʽ����ʱ��Һ��pH���±���
| ������ |
|
|
|
| ��ʼ���� | 2.3 | 7.6 | 3.4 |
| ��ȫ���� | 4.1 | 9.2 | 5.2 |
��ش��������⣺
��1��д�������������ʱ��Һ�з��������ӷ�Ӧ����ʽ��__________
��2������̼���Ƶ���pH��a��a�ķ�Χ��__________��
��3������ʵ��Լ�X��__________
��4������I����3������ʵ�������������__________��__________�ͼ�ѹ���ˡ�
��5���Ƶõ�CoCl2·6H2O���ѹ��ɵ�ԭ����__________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com