
��10�֣�ij��ѧ�о���ѧϰС�����һ�����ԭ��(�����ֶ����ڵij�������������ɵĺϽ��ĩ)����̽�������������̽�����档
��̽��Ŀ�ġ�̽�������ԭ�ϵ����
�����ϼ������� Mg2�����鷽����ȡ2�δ���Һ������2��2 mol��L��1 NaOH��Һ���ټ���1��þ�Լ�(��)Ⱦ��(��������ż��������)�������ֳ���������þ�Լ�(��)Ⱦ�ϳ�����ɫ����ʾ����Һ�к���Mg2����Ag����Cu2����Fe3����NH�����Mg2�������
�� Mg(OH)2������Ũ���Ȼ����Һ�������ij������ܼ��������Ȼ�李�
�ۺܶ�Ͻ��ǽ����������ȷ���Ļ�ѧ��ɡ�
��̽��˼·����ȷ�����ԭ�������������ࣻ�ڲⶨ���ԭ�ϵĻ�ѧʽ��
��ʵ��̽����
��1����ͬѧ���ʵ�鷽����ȷ�����ԭ���еĽ������࣬ʵ���¼���¡�
�ɼ�ʵ���¼��֪�������ԭ������________��________���ֽ�����ɵĺϽ�ʵ������Һ������������������Һ������У���е�����������������
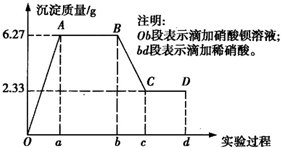
��2����ͬѧ���ü�ͬѧ�Ľ��ۣ��������ͼ��ʾ��ʵ�鲽�裬ȷ���Ͻ���ɡ�
�������ۣ�
����ȷ���Ͻ���ɵ���������________��(����ĸ)
A. m��n������������������B. m��y������������������C. n��y
�����Ͻ������ԭ��������С�Ľ��������ʵ�������Ϊx�����������ʵ���Ϊ7 mol��������ͼ������y��x�仯�����ߡ�
�۵�y��8.5 molʱ���úϽ���һ�ֽ���������仯ѧʽΪ________________��
 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij��ѧ�о���ѧϰС���ij��ɫˮ���ijɷֽ��м��飬��֪��ˮ����ֻ���ܺ���K+��Mg2+��Fe3+��Cu2+��Al3+��Ag+��Ca2+��CO
ij��ѧ�о���ѧϰС���ij��ɫˮ���ijɷֽ��м��飬��֪��ˮ����ֻ���ܺ���K+��Mg2+��Fe3+��Cu2+��Al3+��Ag+��Ca2+��CO2- 3 |
2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2011?̩��һģ��ij��ѧ�о���ѧϰС��Ϊ̽��ijƷ�ƻ������в�����֬����ĺ���������������ʵ�飺
��2011?̩��һģ��ij��ѧ�о���ѧϰС��Ϊ̽��ijƷ�ƻ������в�����֬����ĺ���������������ʵ�飺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com