
| A. | 生成乙烯的是氢氧化钾的水溶液 | B. | 生成乙醇的是氢氧化钾的水溶液? | ||
| C. | 生成乙烯的是在170℃下进行的 | D. | 生成乙醇的是氢氧化钾的醇溶液? |
分析 溴乙烷在KOH的醇溶液中加热可发生消去反应生成乙烯,而溴乙烷在KOH的水溶液中加热可发生水解反应生成乙醇,以此来解答.
解答 解:A.溴乙烷转化为乙烯,为消去反应,条件为KOH的醇溶液、加热,故A错误;
B.生成乙醇为水解反应,条件为KOH的水溶液、加热,故B正确;
C.卤代烃在KOH的醇溶液中加热可发生消去反应,不需要控制温度为170℃,故C错误;
D.卤代烃在KOH的水溶液中加热可发生水解反应,则生成乙醇的是氢氧化钾的水溶液,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意卤代烃的性质及应用,题目难度不大.


科目:高中化学 来源: 题型:推断题



 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
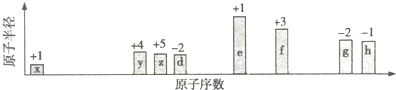
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲基的电子式  | B. | 乙烯的结构简式 CH2CH2 | ||
| C. | 聚丙烯的结构简  | D. | 葡萄糖的实验式(最简式)CH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
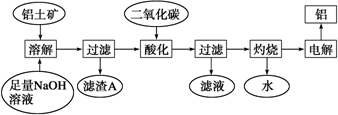
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚):滴入适量的氢氧化钠溶液,振荡,分液 | |
| B. | 苯酚钠(氯化钠):通入过量的CO2,过滤后在沉淀中加入烧碱溶液 | |
| C. | 乙酸乙酯(乙醇):加入适量饱和碳酸钠溶液,振荡,分液 | |
| D. | 硬脂酸钠(甘油\烧碱和水):加入食盐细粒充分搅拌,静置后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol 任何气体的体积都约是22.4L | |
| B. | 18gNH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量与H3PO4的摩尔质量在数值上相等 | |
| D. | 标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
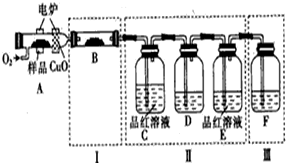
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com