
| A. | NaHSO4是一种酸 | |
| B. | NaHSO4溶液与Cu(OH)2反应的离子方程式:Cu(OH)2+2H+=Cu2++2H2O | |
| C. | NaHSO4溶液可使石蕊试液变蓝 | |
| D. | NaHSO4溶液与MgCl2溶液,BaCl2溶液反应均可生成白色沉淀 |
分析 NaHSO4为酸式盐,由电离方程式NaHSO4=Na++H++SO4 2-可知溶液呈酸性,可与碱、酸碱指示剂反应,电离产生SO4 2-,可与氯化钡反应生成沉淀硫酸钡沉淀,以此解答该题.
解答 解:A.NaHSO4是一种酸电离产生阳离子不仅仅为氢离子,则为酸式盐,不是酸,故A错误;
B.NaHSO4溶液呈酸性,与氢氧化铜发生中和反应,离子方程式为Cu(OH)2+2H+=Cu2++2H2O,故B正确;
C.溶液呈酸性,可使石蕊试液变红色,故C错误;
D.与氯化镁不反应,可与氯化钡反应生成硫酸钡沉淀,故D错误.
故选B.
点评 本题综合考查离子反应,为高频考点,侧重于学生的分析能力的考查,注意把握物质的性质以及离子方程式的书写与判断,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
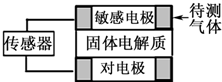 气体自动化检测的探头应用了原电池原理:气体扩散进入敏感电极,发生原电池反应产生电信号,传感器通过对电信号进行分析、判断从而得到结论.如表列出了部分待测气体及敏感电极上部分产物.下列有关说法正确的是( )
气体自动化检测的探头应用了原电池原理:气体扩散进入敏感电极,发生原电池反应产生电信号,传感器通过对电信号进行分析、判断从而得到结论.如表列出了部分待测气体及敏感电极上部分产物.下列有关说法正确的是( ) | 待测气体 | 部分电极反应产物 |
| NO | N2 |
| H2 | H2O |
| CO | CO2 |
| SO2 | SO3 |
| A. | 检测上述气体时,电流均从对电极流向敏感电极 | |
| B. | 检测汽车尾气中的CO时,传感器中通过的电流越大,尾气中CO的含量越高 | |
| C. | 检测SO2时,对电极充入空气,对电极上的电极反应为O2+4H++4e-═2H2O | |
| D. | 检测NO时,敏感电极的电极反应式为:2NO-4e-=N2+2O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给定条件下,Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg,物质间转化能一步实现 | |
| B. | 工业上,常用电解熔融AlCl3的方法冶炼金属铝 | |
| C. | 火法炼铜:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,其中Cu2S既作氧化剂又作还原剂 | |
| D. | 铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,反应物刚好完全反应,反应后固体质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
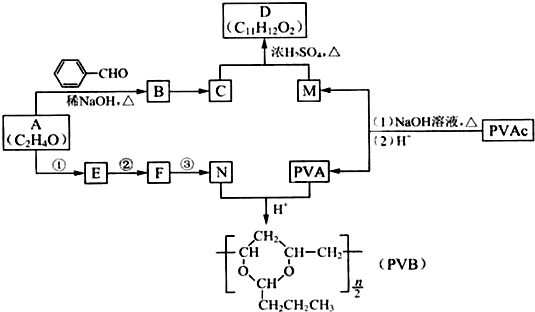
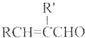 +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)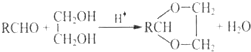
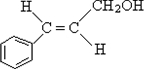 .
.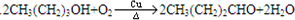 .
.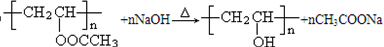 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3是两性氧化物,既能与所有的酸反应,也能与所有的碱反应 | |
| B. | 铝制容器可盛装热的浓H2SO4 | |
| C. | 明矾[KAl(SO4)2•12H2O]的水溶液能够杀菌消毒,可用做净水剂 | |
| D. | 向AlCl3溶液中加入过量氨水后,蒸干并灼烧可得到Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某蓄电池如图所示,以多硫化钠(Na2Sx)、溴化钠(NaBr)水溶液为电解液及电池电化学反应活性物质,电池充放电所发生的反应为2NaBr+(x-1)Na2Sx$?_{充电}^{放电}$Br2+xNa2S(x-1),x为2~4.下列有关判断错误的是( )
某蓄电池如图所示,以多硫化钠(Na2Sx)、溴化钠(NaBr)水溶液为电解液及电池电化学反应活性物质,电池充放电所发生的反应为2NaBr+(x-1)Na2Sx$?_{充电}^{放电}$Br2+xNa2S(x-1),x为2~4.下列有关判断错误的是( )| A. | 电池放电时M为负极 | |
| B. | 电池放电时,N极区c(Na+)不断增加 | |
| C. | 电池充电时,A应接外电源的负极 | |
| D. | 电池充电时N极的电极反应式为(x-1)Sx2-+2e-═xS(x-1)2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com