
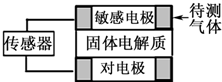
 气体自动化检测的探头应用了原电池原理:气体扩散进入敏感电极,发生原电池反应产生电信号,传感器通过对电信号进行分析、判断从而得到结论.如表列出了部分待测气体及敏感电极上部分产物.下列有关说法正确的是( )
气体自动化检测的探头应用了原电池原理:气体扩散进入敏感电极,发生原电池反应产生电信号,传感器通过对电信号进行分析、判断从而得到结论.如表列出了部分待测气体及敏感电极上部分产物.下列有关说法正确的是( ) | 待测气体 | 部分电极反应产物 |
| NO | N2 |
| H2 | H2O |
| CO | CO2 |
| SO2 | SO3 |
| A. | 检测上述气体时,电流均从对电极流向敏感电极 | |
| B. | 检测汽车尾气中的CO时,传感器中通过的电流越大,尾气中CO的含量越高 | |
| C. | 检测SO2时,对电极充入空气,对电极上的电极反应为O2+4H++4e-═2H2O | |
| D. | 检测NO时,敏感电极的电极反应式为:2NO-4e-=N2+2O2- |
分析 A.电流从正极流向负极;
B.产生的电流大小与失电子多少有关;
C.氧气在正极上得电子生成O2-;
D.根据N元素的化合价判断得失电子.
解答 解:A.失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极,根据待测气体和反应产物可知,部分气体中元素化合价上升,部分气体中元素的化合价下降,所以敏感电极不一定都做电池负极,所以电流不一定都从对电极流向敏感电极,故A错误;
B.产生的电流大小与失电子多少有关,即与电极反应物的含量有关,所以检测汽车尾气中的CO时,传感器中通过的电流越大,尾气中CO的含量越高,故B正确;
C.检测SO2时,对电极充入空气,氧气得电子生成O2-,所以对电极上的电极反应为O2+4e-═2O2-,故C错误;
D.检测NO时,NO转化N2,NO得电子发生氧化反应,所以敏感电极的电极反应式为:2NO+4e-=N2+2O2-,故D错误;
故选B.
点评 本题考查了原电池原理,题目难度中等,根据元素化合价变化确定正负极,正确判断正负极是解本题关键,难点是电极反应式的书写,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下2.24LO2 | B. | 含NA个氢原子的H2 | ||
| C. | 22gCO2 | D. | 含3.01×1023个分子的CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,在0.10mol•L-1CH3COOH溶液中加入少量CH3COONa晶体,能使CH3COOH的电离度降低,溶液的pH增大 | |
| B. | 常温下向氯化铵溶液中加入少量氨水使溶液中c(NH4+)=c(Cl-),则混合液的pH=7 | |
| C. | pH均为5 的盐酸和硫酸氢钠溶液中,水的电离程度后者大 | |
| D. | pH=3的0.1 mol•L-1HA溶液与0.05 mol•L-1NaOH溶液等体积混合后所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
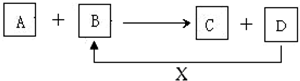
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 | |
| B. | 西非国家曾爆发埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| C. | 硅胶可用作食品干燥剂 | |
| D. | 燃料脱硫,脱氮都是减少酸雨的有效措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、四氯化碳、无水乙醇、己烯 溴水 | |
| B. | MnO2、FeS、CuO、CuS 稀硫酸 | |
| C. | 甲酸、乙酸、乙醛、乙醇 新制氢氧化铜悬浊液 | |
| D. | 苯酚溶液、甲苯、乙酸乙酯、乙酸 饱和碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
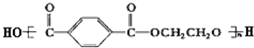
| A. | 合成涤纶纤维的单体为HOCH2CH2OH和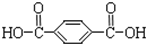 | |
| B. | 棉花和涤纶纤维在一定条件下均能水解 | |
| C. | 涤纶纤维和棉花均为混合物 | |
| D. | 棉花和涤纶纤维不能用燃烧法区别 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题



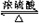 CH3COOCH2CH3+H2O;反应类型:酯化反应.
CH3COOCH2CH3+H2O;反应类型:酯化反应. ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4是一种酸 | |
| B. | NaHSO4溶液与Cu(OH)2反应的离子方程式:Cu(OH)2+2H+=Cu2++2H2O | |
| C. | NaHSO4溶液可使石蕊试液变蓝 | |
| D. | NaHSO4溶液与MgCl2溶液,BaCl2溶液反应均可生成白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com