
根据金属活动性顺序,Ag不能发生反应:2HCl +2Ag =2AgCl+H2↑。但选择恰当电极材料和电解液进行电解,这个反应就能变为现实。下列四组电极和电解液中,为能实现该反应最恰当的是( )
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:单选题
用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入0.1mol Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH (不考虑二氧化碳的溶解)。则电解过程中转移的电子的物质的量为:
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于下图所示原电池装置的叙述中,正确的是( ) 
| A.铜片作负极,质量逐渐减小 | B.溶液的pH逐渐减小 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
按下图所示装置进行有关实验,则下列叙述正确的是
| A.甲装置用作原电池时,锌为正极 |
| B.甲装置用作原电池时,银棒上发生:Ag+ +e-= Ag |
| C.乙装置用作铜片镀镍时,镍作阴极 |
| D.实现铜片表面镀镍时,可将甲中锌棒与乙中铜片相连,甲中银棒与乙中镍片相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于原电池的叙述中,正确的是( )
| A.把电能转化为化学能,使溶液发生氧化还原反应 |
| B.电子从活泼金属流向不活泼金属,不活泼金属为负极 |
| C.外电路中电子从负极流向正极 |
| D.正极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(14分)原电池是化学对人类的一项重大贡献。(1)①某兴趣小组为研究原电池原理,设计如图装置。a和b不连接时,烧杯中发生反应的离子方程式是__________。
②a和b用导线连接,Cu极为原电池__________极(填“正”或“负”),电极反应式是__________。Zn极发生__________(填“氧化”或“还原”)反应。溶液中H+移向__________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻了__________g。
(2)有同学想把Ba(OH)2?8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z和M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为( )
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是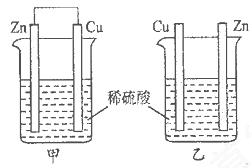
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的酸性均减弱 | D.产生气泡的速率甲比乙慢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com