
(14分)原电池是化学对人类的一项重大贡献。(1)①某兴趣小组为研究原电池原理,设计如图装置。a和b不连接时,烧杯中发生反应的离子方程式是__________。
②a和b用导线连接,Cu极为原电池__________极(填“正”或“负”),电极反应式是__________。Zn极发生__________(填“氧化”或“还原”)反应。溶液中H+移向__________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻了__________g。
(2)有同学想把Ba(OH)2?8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”)。
(1)①Zn+2H+=Zn2++H2↑;②正;2H++2e-=H2↑;氧化;Cu;6.5g;(2)否
解析试题分析:(1)①a和b不连接时,由于Zn的活动性在H的前边,所以Zn能够与酸发生置换反应产生氢气。在烧杯中发生反应的离子方程式是①Zn+2H+=Zn2++H2↑;②若a和b用导线连接,则形成了原电池,Zn是负极,发生氧化反应;Cu极为正极。电极反应式是2H++2e-=H2↑;根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液中H+移向负电荷较多的正极Cu电极移动。③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则由于Zn是+2价的金属,所以理论上Zn片消耗0.1mol,质量减轻了6.5g;(2)有同学想把Ba(OH)2?8H2O晶体与NH4Cl晶体的反应设计成原电池,因为该反应不是氧化还原反应,所以不可行。
考点:考查原电池的反应原理及金属的腐蚀的知识。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:单选题
在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为
A.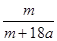 ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D.71m/161(m+9a) ×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
| A.锌为正极,空气进入负极反应 |
| B.负极反应为Zn+2OH--2e-=ZnO+H2O |
| C.正极发生氧化反应 |
| D.电解液肯定是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据金属活动性顺序,Ag不能发生反应:2HCl +2Ag =2AgCl+H2↑。但选择恰当电极材料和电解液进行电解,这个反应就能变为现实。下列四组电极和电解液中,为能实现该反应最恰当的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对如图所示的实验装置的判断中错误的是 
| A.若X为碳棒,开关K置于A处可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法 |
| D.若X为碳棒,开关K置于B处时, |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是
| A.每生成1 mol Na2Mn5O10转移2 mol电子 | B.正极反应式:Ag+Cl--e-=AgCl |
| C.Na+不断向“水”电池的负极移动 | D.AgCl是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是
| A.负极反应式为:H2+2OH- -2e- =2H2O |
| B.正极反应式为:O2 +4H+十4e- =2H2O |
| C.工作一段时间后,KOH溶液的浓度不变 |
| D.电池工作时,电子由正极通过外电路流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图是甲醇/过氧化氢燃料电池内部结构示意图。 工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能。下列说法不正确的是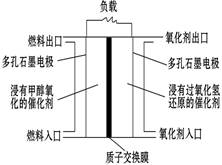
| A.该电池的正极反应式:H2O2+2H++2e—=2H2O |
| B.燃料腔中的多孔石墨电极为该燃料电池的负极,负极产生的H+通过质子交换膜流向正极 |
| C.电池工作时,1 mol甲醇被氧化有6 mol电子转移 |
| D.电路中的电子经正极、负极、质子交换膜后再回到正极,形成闭合回路 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
| A.HCl | B.K2SO4 | C.CuSO4 | D.KCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com