
���� ��1���������ˮ���а�ɫ������̼���������ˮ���������ᣬ���ᱵ�ǰ�ɫ�����������ᣬ�ϲ���ҺΪ��ɫ������ͭ��Һ����ɫ��Һ����һ����CuSO4��
��2�����ð�ɫ��������ϡ������ܽ⣬˵�������ɷ�Ϊ̼��ƺ����ᱵ�������ж�һ������CaCO3��Na2SO4��BaCl2��KNO3����ȷ�����������ʵ����֤�����ӵĴ�������������صĴ��ڣ�
��� �⣺��1���������ˮ���а�ɫ������������һ�����ĩ������CaCO3��Na2SO4��KNO3��BaCl2��CuSO4�е�һ�ֻ�����ɣ�����̼���������ˮ���������ᣬ���ᱵ�ǰ�ɫ�����������ᣬ�ϲ���ҺΪ��ɫ������ͭ��Һ����ɫ��Һ����һ����CuSO4����������ΪCaCO3��BaSO4���������ᱵ�������ƺ��Ȼ���������Ӧ���ɣ�
��2�����ð�ɫ��������ϡ������ܽ⣬˵�������ɷ�Ϊ̼��ƺ����ᱵ������̼��������ᣬ̼�ᱵ�������ᣬ�ж�һ������CaCO3��Na2SO4��BaCl2��KNO3����ȷ�����������ʵ����֤�����ӵĴ�������������صĴ��ڣ��ýྻ�IJ�˿����˿պȡ��Һ���ھƾ��ƻ��������գ�����ɫ�ܲ����۲������ɫ����������ɫΪ��ɫ�������KNO3����֮���ڣ�
�����������÷�ĩ��һ����CaCO3��Na2SO4��BaCl2��һ��û��CuSO4������ȷ������KNO3���������Ƿ���ڿ������ʵ��Ϊ���ýྻ�IJ�˿����˿պȡ��Һ���ھƾ��ƻ��������գ�����ɫ�ܲ����۲������ɫ����������ɫΪ��ɫ�������KNO3����֮���ڣ���Ӧ�����ӷ���ʽΪ��SO42-+Ba2+=BaSO4����CaCO3+2H+=Ca2++H2O+CO2����
�ʴ�Ϊ��CaCO3��Na2SO4��BaCl2��CuSO4��KNO3��SO42-+Ba2+=BaSO4����CaCO3+2H+=Ca2++H2O+CO2����
���� ���⿼�����������ʵķ�������Ӧ��������ӹ��������Ӧ�ã���Ҫ�dz����ܽ��ԡ���Һ��ɫ�������仯�жϣ���Ŀ�ϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
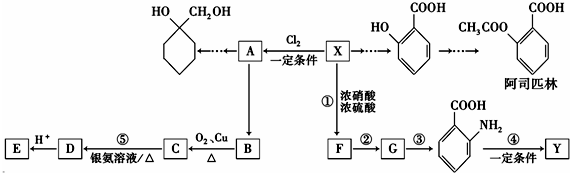
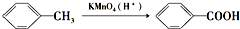
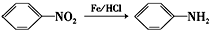 ���������ױ�������
���������ױ�������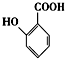 ������Ϊ���ǻ������ᣬG�й���������Ϊ�������Ȼ���
������Ϊ���ǻ������ᣬG�й���������Ϊ�������Ȼ��� ��
�� $\stackrel{һ��������}{��}$
$\stackrel{һ��������}{��}$ +��n-1��H2O��
+��n-1��H2O��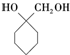 �ĺϳ�·�ߣ����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·�ߣ����Լ����ã����ϳ�·������ͼʾ�����£�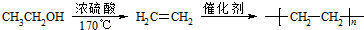
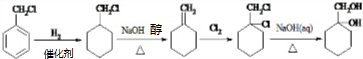 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ��ʼ����ʱpH | ��ȫ����ʱpH |
| Fe��OH��3 | 2.7 | 3.7 |
| Fe��OH��2 | 7.6 | 9.6 |
| Cu��OH��2 | 5.2 | 6.4 |
| ������ | ����pH������ | ||
| A | ˫��ˮ | E | ��ˮ |
| B | ������� | F | ��ʽ̼��ͭ |
| C | ��ˮ | G | ����ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1MgCl2��Һ�к��е�Mg2+��Ŀһ��С��0.1NA | |
| B�� | ��״���£�11.2 L CCl4�к��еķ�����ĿΪ0.5NA | |
| C�� | 4.6g��NO2��N2O4��ɵĻ�����к�����ԭ�ӵ���ĿΪ0.2 NA | |
| D�� | 1 mol CH5+�к��еĵ�����ĿΪ11NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ������ķ�Ӧ OH-+H+�TH2O | |
| B�� | ��CaCl2��Һ��ͨ��������CO2 Ca2++CO2+H2O�TCaCO3��+2H+ | |
| C�� | ͭƬ������������Һ�� Cu+Ag+�TCu2++Ag | |
| D�� | ̼�������ϡ������ CaCO3+2H+�TCa2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2N2H4��g��+2NO2��g���T3N2��g��+4H2O��l����H=-1135.7 kJ•mol-1 | |
| B�� | 2N2H4��g��+2NO2��g���T3N2��g��+4H2O��g����H=-1000.3 kJ•mol-1 | |
| C�� | N2H4��g��+NO2��g���T$\frac{3}{2}$N2��g��+2H2O��l����H=-1135.7 kJ•mol-1 | |
| D�� | 2N2H4��g��+2NO2��g���T3N2��g��+4H2O��g����H=-1135.7 kJ•mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 34Sԭ�Ӻ��ڵ�������Ϊ16 | B�� | 16O��18O����ͬλ�� | ||
| C�� | 13C��15Nԭ�Ӻ��ڵ����������2 | D�� | 2H�ĺ����������1H��һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�16gO2������ԭ����NA | |
| B�� | ��״���£�2.24Lˮ�����ĵ�����Ϊ10NA | |
| C�� | 2.4g����þ���������ᷴӦʧȥ������0.2NA | |
| D�� | 1.6g���麬�й��õ��Ӷ���Ŀ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Ӵ�������������춡����� | |
| B�� | ��������ȶ��Դ����춡�� | |
| C�� | �춡��ת��Ϊ������Ĺ�����һ�����ȹ��� | |
| D�� | �춡������е�̼�����������Ķ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com