
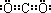 ;(2)过滤;水(或乙醇)(3)Si+2OH﹣+H2O═SiO32﹣+2H2↑;0.17 mol?L﹣1(4)③④
;(2)过滤;水(或乙醇)(3)Si+2OH﹣+H2O═SiO32﹣+2H2↑;0.17 mol?L﹣1(4)③④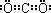 ,故答案为:第二周期第ⅣA族;氧(或O);
,故答案为:第二周期第ⅣA族;氧(或O);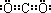 ;
;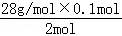 =1.4g,
=1.4g,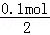 ="0.05" mol,
="0.05" mol,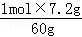 =0.12mol,
=0.12mol,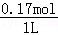 =0.17mol/L,
=0.17mol/L,

科目:高中化学 来源:不详 题型:单选题
| A.NH3、O2、HCl | B.N2、H2SCl2 |
| C.CO2、NO、O2 | D.N2、O2、CO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 常温下铁与浓硫酸、浓硝酸均不反应 | 可用铁槽车密封运送浓硫酸、浓硝酸 |
| B | H2O2、SO2都能使酸性KMnO4褪色 | H2O2表现还原性,SO2表现漂白性 |
| C | Al有还原性 | 利用铝热反应冶炼金属Mn |
| D | 将水蒸气通过灼热的铁粉,铁粉变红褐色 | 铁粉与水蒸气反应生成Fe2O3 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢氟酸能和玻璃的成分SiO2发生化学反应 |
B.根据SiO2+Na2CO3 Na2SiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强 Na2SiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强 |
| C.CO2气体通入到Na2SiO3溶液中可以制得硅酸 |
| D.原硅酸不稳定,易失去水分子成为硅酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.聚二氧化碳塑料是通过聚合反应制得的 |
| B.聚二氧化碳塑料与干冰互为同素异形体 |
| C.聚二氧化碳塑料与干冰都属于纯净物 |
| D.聚二氧化碳塑料的使用会产生白色污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.处理宇航员的生活垃圾 | B.去除呼吸废气中的异味 |
| C.提供生活中需要的能量 | D.改善失重条件下的平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com