
【题目】某温度时,浓度均为1mol·L-1的两种气体X2和Y2,在恒容密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4mol·L-1,Y2的浓度为0.8mol·L-1,生成的Z的浓度为0.4mol·L-1,则该反应的化学方程式(Z用X、Y表示)是
A.X2+2Y2![]() 2XY2B.2X2+Y2
2XY2B.2X2+Y2![]() 2X2Y
2X2Y
C.X2+3Y2![]() 2XY3D.3X2+Y2
2XY3D.3X2+Y2![]() 2X3Y
2X3Y
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
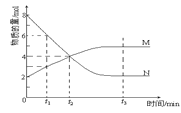
A.反应的化学方程式:2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下列试管实验操作及现象,得出“实验结论”正确是
选项 | 试管实验操作及现象 | 实验结论 |
A | 向某溶液中加入AgNO3溶液,有白色沉淀生成 | 该溶液中一定含有Cl- |
B | 向某溶液中加入稀盐酸,有无色气体产生 | 该溶液中一定含有 |
C | 向某溶液中加入盐酸无现象,再加入BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有 |
D | 向某溶液中加入稀氢氧化钠,用湿润的红色石蕊试纸靠近试管口,试纸未变蓝。 | 该溶液中一定不含 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学中常见的物质,且A、B、C均含有同一种元素,在一定条件下相互转化关系如下图所示(部分产物已略去)。请回答:
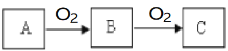
(1)若B是无色气体,C是红棕色气体。
① A、B、C所含相同元素在元素周期表中的位置是______。
② 下列说法正确的是______(填字母)。
a.常温下,A为无色气体
b.A、B、C中所含相同元素的化合价依次升高
c.C与水反应只做还原剂。
③若A是化合物,写出由A氧化生产B的化学方程式__________________。
(2)若B是一种有刺激性气味的有毒气体,C与水反应生成硫酸
① A、B、C所含相同元素的原子结构示意图是______。
② 下列说法不正确的是______(填字母)。
a.A一定是黄色晶体
b.可以用上述转化关系制备硫酸
c.B与水反应做还原剂。
③C的水溶液与氢氧化钠的反应为______________(填吸热或放热)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应2Fe3++Cu=2Fe2++Cu2+ 设计成如图所示原电池,可供选择的电解质溶液有FeCl3、CuSO4两种溶液。
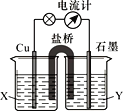
(1)石墨是电池的________极,X应选________溶液,Y应选___________________溶液。
(2)正极上的电极反应式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如图:

下列说法不正确的是( )
A.石灰石、纯碱、石英都属于盐,都能与盐酸反应
B.用铝土矿制备较高纯度Al的过程中常用到NaOH溶液、CO2、冰晶石等
C.在制粗硅时,被氧化的物质与被还原的物质的物质的量之比为2:1
D.黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | Na2S溶液滴入AgCl浊液中 | 热铜丝插入稀硝酸中 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 沉淀由白色逐渐变为黑色 | 产生无色气体,随后变为红棕色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1000mol·L-1(NH4)2SO4溶液中逐滴加入0.2000mol·L-1NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发)。下列说法正确的是( )
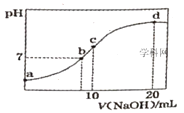
A.点a所示溶液中:c(NH4+)=2c(SO42-)>c(OH-)>c(H+)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-)
C.点c所示溶液中:c(SO42-)+c(H+)=c(NH3H2O)+c(OH-)
D.点d所示溶液中:c(SO42-)>c(NH3·H2O)>c(OH-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(COCl2)常作有机合成、农药、药物、燃料及其他化工制品的中间体。
(1)COCl2结构与甲醛相似,写出COCl2电子式_____;解释COCl2的沸点比甲醛高的原因是_____。
(2)密闭容器中吸热反应COCl2(g)![]() Cl2(g)+CO(g)达到平衡后,改变一个条件,各物质的浓度变化如图所示(10~14min时有一物质浓度变化未标出)。
Cl2(g)+CO(g)达到平衡后,改变一个条件,各物质的浓度变化如图所示(10~14min时有一物质浓度变化未标出)。
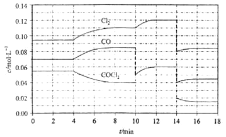
①说明该反应已达到平衡状态的是_____。
a.C(COCl2)=C(Cl2)
b.正(COCl2)=逆(CO)
c.容器内温度保持不变
d.容器内气体密度保持不变
②4~10min平均反应速率v(COCl2)为_____;10min时改变的反应条件是_____。
③0~4min、8~10min和16~18min三个平衡常数依次为K1、K2、K3,比较其大小____;说明理由____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com