
【题目】有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是_________和_________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时,产生蓝色沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解,剩余白色固体,则X为 (填序号)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2gCu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式 。
若要将Cu完全溶解,至少加入H2SO4的物质的量是 。
(4)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
【答案】
(1)K2CO3 Ba(OH)2;
(2)B;
(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;0.4mol;
(4)2Fe3++2I-=2Fe2++I2;
【解析】
试题分析:CO32-与Cu2+、Ba2+、Fe3+、Al3+不能大量共存,OH-与Fe3+、Al3+、Cu2+不能大量共存,则必有的两种物质记为A、B,A、B分别为K2CO3、Ba(OH)2,C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,蓝色沉淀为氢氧化铜,白色沉淀为硫酸钡,则A应为Ba(OH)2,C中含SO42-,则C为CuSO4,D为Al(NO3)3,E为FeCl3。
(1)由上述分析可知,必有的两种物质为K2CO3、Ba(OH)2,故答案为:K2CO3;Ba(OH)2;
(2)由上述分析可知,C为CuSO4,C中X为SO42-,故答案为:B;
(3)根据以上推断可知D中含有NO3-,已知将19.2gCu投入装有足量D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,发生的反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,则n(Cu)=mM=![]() =0.3mol,有方程可知
=0.3mol,有方程可知![]() =
=![]() ,所以n(H+)=0.8mol,所以n(H2SO4)=12n(H+)=0.4mol,故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol;
,所以n(H+)=0.8mol,所以n(H2SO4)=12n(H+)=0.4mol,故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol;
(4)E为FeCl3,E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2。


科目:高中化学 来源: 题型:
【题目】某工业废液中含有Cu2+、Mg2+、Zn2+等离子,为将其回收利用,再采用了如下工艺
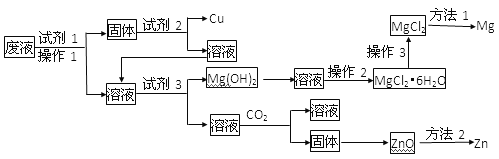
已知Zn(OH)2的性质与Al(OH)3相似
所用试剂在下列试剂中选择
① 铁粉 ②锌粉 ③稀HNO3 ④稀H2SO4 ⑤稀HCl ⑥稀氨水 ⑦NaOH溶液 ⑧石灰水
请回答下列问题:
(1)试剂1、试剂2、试剂3分别可以是________、________、________(填编号)
(2)操作2是_______________、______________、______________
(3)操作3是________________________________
(4)加过量CO2时发生反应的离子方程式________________________
(5)用离子方程式解释试剂3能分离出Mg(OH)2的原理:__________________、_________________
(6)在金属冶炼方法中方法1是_________方法2是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“绿色化学工艺”中,理想状态是原子利用率为100%。在用CH3C≡CH合成CH2===C(CH3)COOCH3的过程中,欲使原子利用率达到最高,还需要其他的反应物有( )
A.H2和CO2 B.H2O和CO2 C.H2和CH3OH D.CO和CH3OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)取一定量的Na2CO3、NaHCO3和Na2SO4混合物与250mL 1.00mol·L-1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100mol·L-1Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL 1.00mol·L-1盐酸恰好完全中和。计算:
(1)混合物中Na2SO4的质量; (2)混合物中Na2CO3的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述正确的是( )
A.煤的干馏和煤的液化均是物理变化
B.海水淡化的方法有蒸馏法、电渗析法等
C.棉、丝、毛、油脂都是天然有机高分子化合物
D.石油裂化的目的是得到乙烯、丙烯等化工原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.氯化铝与过量氨水:Al3+ +4OH-=AlO2- +H2O
B.钠和冷水反应:Na+2H2O =Na++2OH+H2↑
C.氯气与水反应Cl2+H2O![]() Cl- + H++HClO
Cl- + H++HClO
D.碳酸钙与盐酸反应:CO32-+ 2H+ = H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸及其盐在工业上具有广泛的用途。下面来解释亚硫酸及其盐的有关性质的方程式正确的是
A.亚硫酸水溶液的pH<7:H2SO3![]() 2H++SO32-
2H++SO32-
B.将亚硫酸滴入饱和Na2CO3溶液有气泡产生:2H++CO32-=H2O+CO2↑
C.Na2SO3溶液能使红色石蕊变蓝:SO32-+H2O=HSO3-+OH-
D.Na2SO3溶液中加入足量的酸化Ba(NO3)2溶液出现白色沉淀:
3SO32-+2NO3-+2H++3Ba2+=3BaSO4↓+2NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系 如图所示,下列说法中不正确的是( )

A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.25 mol
D.K2Cr2O7与FeSO4开始反应时物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.离子键没有方向性和饱和性,而共价键有方向性和饱和性
B.离子键的强弱主要决定于离子半径和离子所带电荷数
C.配位键在形成时,由成键双方各提供一个电子形成一对共用电子
D.金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com