
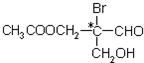 是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )
是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液反应 | ||
| C. | 催化剂作用下与H2反应 | D. | 与银氨溶液作用发生银镜反应 |
分析 根据题意知,手性碳原子连接4个不同的原子或原子团,如果反应后的生成物的碳原子上连接4个不同的原子或原子团,则其生成物就含有手性碳原子,以此解答该题.
解答 解:A.该有机物与乙酸反应生成的酯中,原来的手性碳原子现在连接两个CH3COOCH2-,所以没有手性碳原子,故A不选;
B.该有机物与氢氧化钠溶液反应后生成的醇中,原来的手性碳原子现在连接两个-CH2OH,所以没有手性碳原子,故B不选;
C.该有机物在催化剂作用下与氢气反应,原来的手性碳原子现在连接两个-CH2OH,所以没有手性碳原子,故C不选;
D.该有机物与银氨溶液反应后的生成的有机物中,原来的手性碳原子现在连接的原子或原子团是:一个溴原子、一个-CH2OH、一个CH3COOCH2-、一个-COOH,所以该原子仍然是手性碳原子,故D选.
故选D.
点评 本题考查了手性碳原子的判断,为高频考点,明确“手性碳原子连接4个不同的原子或原子团”是解本题的关键,根据有机物的结构来分析解答即可,难度不大.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:多选题
| A. | 8g碳和14g氧气反应生成22g二氧化碳 | |
| B. | 二氧化碳由一个碳原子和两个氧原子构成 | |
| C. | 1g硫和1g氧气反应生成2g二氧化硫 | |
| D. | 水银温度计在温度升高时水银柱上升是因为汞原子的体积变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A是一种淡黄色固体,B是造成酸雨的“罪魁祸首”,则X为O2 | |
| B. | 若X是生活中常见的过渡金属,A是黄绿色气体,则B→C的离子方程式为Fe+2Fe3+=3Fe2+ | |
| C. | 若C是一种酸式盐,则X一定是CO2 | |
| D. | A既可以为金属单质,也可以为非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 化学键只存在于分子内,分子间作用力只存在于分子间 | |
| B. | 分子晶体在熔化时,共价键没有被破坏 | |
| C. | 在晶体里有阳离子存在时,不一定有阴离子存在 | |
| D. | 物质在溶于水的过程中,化学键一定会被破坏或改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
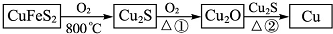
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
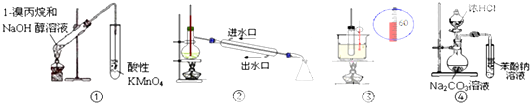
| A. | ①装置用于检验1-溴丙烷消去产物 | B. | ②装置用于石油的分馏 | ||
| C. | ④装置可证明酸性:盐酸>碳酸>苯酚 | D. | ③装置用于实验室制硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁条作负极,电极反应:Mg-2e-=Mg2+ | |
| B. | 铝片作负极,电极反应:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 电流从Al电极沿导线流向Mg电极 | |
| D. | 铝片上有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
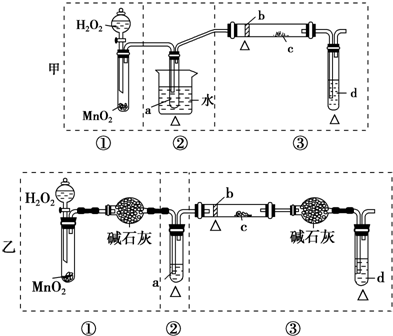
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com