
【题目】下列除去杂质方法正确的是( )
A. 除去CO2中混有的CO:用浓NaOH溶液洗气
B. 除去BaCO3固体中混有的BaSO4:加过量稀盐酸后,过滤、洗涤
C. 除去KNO3溶液中混有的NaCl:蒸发结晶
D. 除去Cu粉中混有的CuO:加适量稀硫酸后,过滤、洗涤
科目:高中化学 来源: 题型:
【题目】关于a g 氢气 和b g氦气,下列说法正确的是( )
A. 同温、同压下,氢气和氦气的体积比是a:2b
B. 同温、同压下,若a=b,则氢气 和氦气的物质的量之比为2:1
C. 体积相同时,氦气的质量一定大于氢气的质量
D. 同温同压下,若二者的物质的量相同,其所含原子数也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.
则下列说法错误的是( )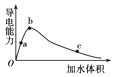
A.醋酸的电离程度:a<b<c
B.溶液的pH值:b<a<c
C.蘸取a点溶液滴在湿润的pH试纸上,测得pH值一定偏大
D.若分别取a、b、c三点的溶液各10 mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种主族元素A、B、C、D、X、Y,其原子序数依次增大,均小于54;常温下A2B呈液态,是食物中主要营养物质之一;高纯C单质具有良好的半导体性能;D、X、Y原子核外最外层电子数均为7;过渡元素Z与B可形成多种化合物,其中红棕色粉末Z2B3常用作外墙涂料.请按要求回答下列问题:
(1)将D2水溶液滴入浅绿色的ZD2溶液中发生反应的离子方程式为 . ①学生甲认为X2和Y2都可能将Z2+氧化为Z3+ , 他推理的依据是 .
②而学生乙认为X2和Y2都不能将Z2+氧化为Z3+;学生丙认为X2能将Z2+氧化为Z3+而Y2不能.学生乙、丙推理的依据是 .
(2)A与B可形成既含极性键又含非极性键的化合物W.W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等.①W的电子式为 , W第一步电离方程式为 .
②如果配制W溶液的水中含有Z3+ , 会削弱W的消毒杀菌能力,甚至会完全失去杀菌作用.试用化学方程式分析其原因: .
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族,原子核外电子层数均小于7;常温下其单质,在空气中锡、锗不反应,而铅表面会生成一层氧化铅,锗与盐酸不反应,而锡与盐酸反应.由此可得出以下结论:①锗的原子序数为;
②它们+4价氢氧化物的碱性由强到弱顺序为(填化学式) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗甲流感药物达菲(Tamiflu)是以莽草酸(A)为原料,经过十步反应合成制得.莽草酸可以从常用的烹调香料“八角”中提取.达菲及A(莽草酸)、B的结构简式如图甲: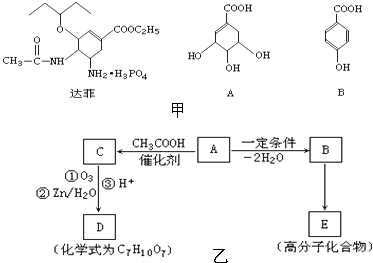
已知: ![]()
化合物A、B、C、D存在如图乙所示的转化关系:
回答下列问题:
(1)写出达菲中含氧官能团的名称:;
(2)写出A→C的反应类型:;
(3)写出B→E的化学方程式:;
(4)写出D的结构简式:;
(5)已知B有多种同分异构体,写出一种符合下列性质的B的同分异构体的结构简式①与FeCl3溶液作用显紫色;
②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种.
(6)设计A生成C的目的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2 . 查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾.
(1)化合物SO2Cl2中S元素的化合价是 .
(2)用二氧化锰和浓盐酸制氯气的化学方程式是 .
(3)在收集氯气前,应依次通过盛有饱和食盐水和的洗气瓶.
(4)用如图所示装置收集满Cl2 , 再通入SO2 , 集气瓶中立即产生无色液体,充分反应后,将液体和剩余气体分离,进行如下研究.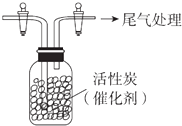
a.研究反应的产物.向所得液体中加水,出现白雾,振荡、静置得到无色溶液.经检验该溶液中的阴离子(除OH﹣外)只有SO ![]() 、Cl﹣ , 证明无色液体是SO2Cl2 .
、Cl﹣ , 证明无色液体是SO2Cl2 .
①写出SO2Cl2与H2O反应的化学方程式 . ②检验该溶液中Cl﹣的方法是 .
b.继续研究反应进行的程度.用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀.
①该白色沉淀的成分是 .
②写出SO2与Cl2反应的化学方程式,并阐述理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是化合物,B是金属单质,它们之间相互反应以及生成物之间的转化关系如图所示: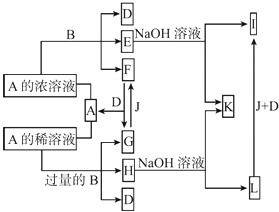
(1)金属B在元素周期表中的位置是 , B和A的浓溶液反应的条件是 . 写出少量B与A的稀溶液反应的离子方程式: .
(2)常温下0.1 mol/L E的水溶液中各离子浓度大小关系为 .
(3)L转化为I的现象是 . 写出有关的化学方程式: .
(4)如何检测H溶液中阳离子的存在,写出实验操作方法、现象、结论: .
(5)已知25℃时Fe(OH)3的Ksp=3.5×10﹣39 , 现将4.0×10﹣8 mol/L E溶液与2.0×10﹣8 mol/L NaOH溶液等体积混合(忽略溶液混合时体积的变化),通过列式计算说明是否有沉淀产生: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影 3 区域的是

A. Cl2+2NaI==2NaCl+I2 B. CH4+2O2![]() CO2+2H2O
CO2+2H2O
C. 4Fe(OH)2+O2+2H2O=4Fe(OH)3 D. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com