
已知一定条件下断裂或生成某些化学键的能量关系如下表:
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量 436kJ |
| 断裂1mol Cl2分子中的化学键 | 吸收能量 243kJ |
| 形成1mol HCl分子中的化学键 | 释放能量 431kJ |
对于反应:H2(g)+ Cl2 (g) = 2HCl (g),下列说法正确的是
A.该反应的反应热 △H > 0
B.生成1mol HCl时反应放热91.5kJ
C.Cl2中的化学键比H2中的化学键更稳定
D.相同条件下,氢气分子具有的能量高于氯气分子具有的能量
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列各项叙述正确的是( )
A.由同种元素组成的物质肯定属于纯净物
B.具有相同质子数的微粒都属于同种元素
C.一种元素可有多种离子,但只有一种电中性的原子
D.含有离子键的化合物一定是离子化合物.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室要用98%(ρ=1.8g·cm-3)的硫酸配制3.68 mol·L-1的硫酸溶液400 mL
(1)需准确量取98%的硫酸 mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液,必须用到的实验仪器是(填写序号):
①500mL量筒 ② 烧杯 ③1000mL容量瓶 ④500mL容量瓶
⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管
(3)将上述一定体积的98%的硫酸溶于水的操作是 。
(4)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,导致所配制的硫酸溶液浓度偏低的是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)可以对饮用水进行净化处理,可由下列方法制得:
Fe2O3+3Na2O2  2Na2FeO4+Na2O,
2Na2FeO4+Na2O,
关于该反应说法正确的是
A.Na2FeO4属于共价化合物
B.反应中Na2O2是氧化剂
C.生成1 mol Na2FeO4,有6 mol 电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷
B.用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
C.用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3
D.油脂在酸性或碱性条件下均能发生水解反应,且产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年9月29日成功发射天宫一号的长征二号F型火箭巨大的推力来源于一个氧化还原反应,反应时偏二甲肼(C2H8N2)做燃料,N2O4做氧化剂,生成三种气体物质,完成并配平该燃烧反应的化学方程式:
C2H8N2 + N2O4 = N2 ↑+ CO2↑ +
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化学方程式是:
,
对上述反应中的各种物质,下列说法正确的是 。
A. N2O4只做氧化剂 B. 产物中两种酸都是强酸
C. 反应中水只做溶剂 D. N2O4泄漏后可产生红棕色气体
(2) 通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:
| 分子中所有的化学键 | 峰面积之比 | |
| 红外光谱 |
|
|
| 核磁共振氢谱 |
| 3:1 |
符合上表结构及数据要求的同分异构体共有 种,已知偏二甲肼的结构中有一个氮原子上没有连接氢原子,则偏二甲肼的结构简式是____ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在体积为V L密闭容器中加入n mol A、2n mol B,发生反应:
A(g)+2B(g) 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1) 一段时间后上述反应达到平衡。则下列说法中正确的是________(双选)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2) K和x的关系满足K=________。在保证A浓度不变的情况下,扩大容器的体积,平衡______(填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(3) 该反应的逆反应速率与时间的关系如图所示。
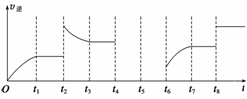
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都只改变了一种条件,试判断改变的条件:
t2时__________________________________________;
t8时__________________________________________。
② t2时平衡向________(填“正反应”或“逆反应”)方向移动。
③ 若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com