
2011年9月29日成功发射天宫一号的长征二号F型火箭巨大的推力来源于一个氧化还原反应,反应时偏二甲肼(C2H8N2)做燃料,N2O4做氧化剂,生成三种气体物质,完成并配平该燃烧反应的化学方程式:
C2H8N2 + N2O4 = N2 ↑+ CO2↑ +
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化学方程式是:
,
对上述反应中的各种物质,下列说法正确的是 。
A. N2O4只做氧化剂 B. 产物中两种酸都是强酸
C. 反应中水只做溶剂 D. N2O4泄漏后可产生红棕色气体
(2) 通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:
| 分子中所有的化学键 | 峰面积之比 | |
| 红外光谱 |
|
|
| 核磁共振氢谱 |
| 3:1 |
符合上表结构及数据要求的同分异构体共有 种,已知偏二甲肼的结构中有一个氮原子上没有连接氢原子,则偏二甲肼的结构简式是____ __。
科目:高中化学 来源: 题型:
有BaCl2和NaCl的混合溶液2.0L,将它平均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl—离子完全沉淀。反应中消耗0.5mol H2SO4、2.0mol AgNO3。据此得知原混合溶液中的c(Na+)为( )
A.0.5 mol·L-1 B.0.75 mol·L-1 C.1.5 mol·L-1 D.1.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定条件下断裂或生成某些化学键的能量关系如下表:
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量 436kJ |
| 断裂1mol Cl2分子中的化学键 | 吸收能量 243kJ |
| 形成1mol HCl分子中的化学键 | 释放能量 431kJ |
对于反应:H2(g)+ Cl2 (g) = 2HCl (g),下列说法正确的是
A.该反应的反应热 △H > 0
B.生成1mol HCl时反应放热91.5kJ
C.Cl2中的化学键比H2中的化学键更稳定
D.相同条件下,氢气分子具有的能量高于氯气分子具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中一定只有共价键
C.W、X、Z三种元素最高价氧化物对应水化物的酸性逐渐减弱
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.只有反应体系中所有分子同时都发生有效碰撞的反应才是放热反应
B.通常条件下能够自发进行的反应必须具备△H和△S均大于0
C.任何化学反应只要是自发进行的放热反应都可以设计成原电池,为外界提供电能
D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配置氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
设某元素原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为wg,此原子的质量为(m+n)wg
D.核内中子的总质量小于质子的总质量
查看答案和解析>>
科目:高中化学 来源: 题型:
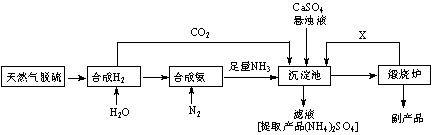
某合成氨厂利用附近化工厂副产品CaSO4设计了以下制备(NH4)2SO4的工艺流程:
 |
请回答以下问题:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,
得到单质硫并使吸收液再生,写出再生反应的化学方程式: 。
(2)工业上在500℃左右使用铁触媒作为催化剂合成NH3,
①铁触媒中含有Fe3+,,则Fe3+的核外电子排布式为
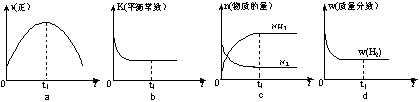
②500℃时,合成塔中的反应为:N2(g)+3H2(g)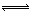 2NH3(g) ∆H= -92.4kJ/mol在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母编号)。
2NH3(g) ∆H= -92.4kJ/mol在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母编号)。
 |
(3)沉淀池中反应的化学方程式为
(4)在上述流程中可以循环使用的X是 (填化学式),从(NH4)2SO4溶液中获得
(NH4)2SO4晶体操作的步骤是是加热浓缩、 、过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com