
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中一定只有共价键
C.W、X、Z三种元素最高价氧化物对应水化物的酸性逐渐减弱
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
科目:高中化学 来源: 题型:
容量瓶是用来配制一定物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容积、④压强、⑤刻度线、这五项中的( )
A.①③⑤ B.③④⑤ C.①②④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是同一周期的五种主族元素,A与B的最高价氧化物对应的水化物呈碱性,且碱性B>A;C和D的气态氢化物的还原性为D>C;五种元素的原子得失电子后所形成的简单离子中E的离子半径最小,则它们的原子序数由小到大的的顺序为( )
A.BAEDC B.CDBAE C.ABCDE D.ECDBA
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)可以对饮用水进行净化处理,可由下列方法制得:
Fe2O3+3Na2O2  2Na2FeO4+Na2O,
2Na2FeO4+Na2O,
关于该反应说法正确的是
A.Na2FeO4属于共价化合物
B.反应中Na2O2是氧化剂
C.生成1 mol Na2FeO4,有6 mol 电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释物质用途或现象的反应方程式不准确的是
A.硫酸型酸雨的形成会涉及反应:2H2SO3+O2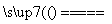 2H2SO4
2H2SO4
B.热的纯碱溶液可以清洗油污的原因: +2H2O
+2H2O
 H2CO3+2OH¯
H2CO3+2OH¯
C.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH¯===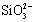 +H2O
+H2O
D.成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl¯+ ClO¯+2H+= Cl2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年9月29日成功发射天宫一号的长征二号F型火箭巨大的推力来源于一个氧化还原反应,反应时偏二甲肼(C2H8N2)做燃料,N2O4做氧化剂,生成三种气体物质,完成并配平该燃烧反应的化学方程式:
C2H8N2 + N2O4 = N2 ↑+ CO2↑ +
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化学方程式是:
,
对上述反应中的各种物质,下列说法正确的是 。
A. N2O4只做氧化剂 B. 产物中两种酸都是强酸
C. 反应中水只做溶剂 D. N2O4泄漏后可产生红棕色气体
(2) 通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:
| 分子中所有的化学键 | 峰面积之比 | |
| 红外光谱 |
|
|
| 核磁共振氢谱 |
| 3:1 |
符合上表结构及数据要求的同分异构体共有 种,已知偏二甲肼的结构中有一个氮原子上没有连接氢原子,则偏二甲肼的结构简式是____ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
医学研究证明,用放射性135 53I治疗肿瘤可收到一定疗效,下列有关135 53I叙述正确的是( )
A.135 53I是碘的一种同素异形体
B.135 53I是一种新发现的元素
C.135 53I位于元素周期表中第4周期ⅦA族
D.135 53I核内的中子数与核外电子数之差为29
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,某稀溶液中由水电离产生的c(H+)=10-13mol/L。有关该溶液的叙述正确的是: ( )
A .该溶液的pH值可能为1 B .水的电离受到促进
C .水的离子积将变小 D. 该溶液的pH值一定为13
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作、现象与所得结论一致的是
| 实验操作 | 现象 | 结论 | |
| A | 向盛有25mL沸水的烧杯中滴加5~6滴FeCl3饱和溶液,继续煮沸 | 溶液生成红褐色沉淀 | 制得Fe(OH)3胶体 |
| B | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液, | 前者溶液变蓝, 后者有黄色沉淀 | KI3溶液中存在平衡: I |
| C | 将溴乙烷和NaOH乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液 褪色 | 产生了乙烯 |
| D | 蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水 | 出现红色沉淀 | 蔗糖水解已水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com