
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]
�����㶹����һ����������Ѫ�ܼ�����ҩ����谭Ѫ˨��չ�������㶹�ؿ���ͨ�����·����ϳ�(���ַ�Ӧ����ʡ��)��
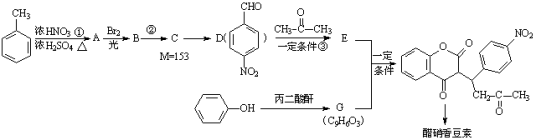
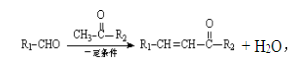
��֪��
�ش���������
��1����Ӧ���ķ�Ӧ������ ����A��B����Ĺ����������� ��
��2����Ӧ���Ļ�ѧ����ʽΪ ��
��3����Ӧ���Ļ�ѧ����ʽΪ ��
��4������E���ʣ�����˵����ȷ���� (����ĸ���)��
a���ں˴Ź������������������շ�
b�����������Ը��������Һ����D��E
c�����Է����ӳɷ�Ӧ���ۺϷ�Ӧ��������Ӧ�ͻ�ԭ��Ӧ
d������˳���칹
��5��д��G�Ľṹ��ʽ ��
��6�����ӽṹ��ֻ����һ��������ͬʱ��������������G��ͬ���칹�干�� �֡�
�������Ȼ�����Һ������ɫ��Ӧ�� ������̼��������Һ��Ӧ���ɶ�����̼���塣
���У������ϵ�һ�ȴ���ֻ�����ֵ�ͬ���칹��Ľṹ��ʽΪ ��
���𰸡���1��ȡ����Ӧ(��������Ӧ) ��ԭ��
��2��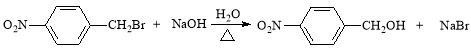
��3��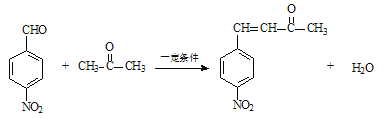
��4��cd ��5��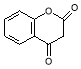 ��6��13
��6��13 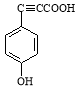
��������
����������ױ������ᷢ��ȡ����Ӧ����A������D�Ľṹ֪��A�ṹ��ʽΪ![]() ��B�Ľṹ��ʽΪ
��B�Ľṹ��ʽΪ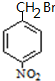 �����C��Է�������֪��C�ṹ��ʽΪ
�����C��Է�������֪��C�ṹ��ʽΪ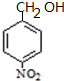 ��D�ͱ�ͪ��Ӧ����E��E�ṹ��ʽΪ
��D�ͱ�ͪ��Ӧ����E��E�ṹ��ʽΪ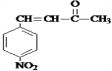 �����Ӻͱ���������Ӧ����G��E��G��Ӧ���ɴ����㶹�أ����ݴ����㶹�ؽṹ��ʽ֪��G�ṹ��ʽΪ
�����Ӻͱ���������Ӧ����G��E��G��Ӧ���ɴ����㶹�أ����ݴ����㶹�ؽṹ��ʽ֪��G�ṹ��ʽΪ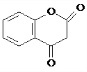 ��
��
��1��ͨ�����Ϸ���֪����Ӧ���ķ�Ӧ������ȡ����Ӧ����������Ӧ����
��2����A��B����Ĺ�������������ԭ�ӣ�
��3����Ӧ���Ļ�ѧ����ʽΪ![]() ��
��
��4����Ӧ���Ļ�ѧ����ʽΪ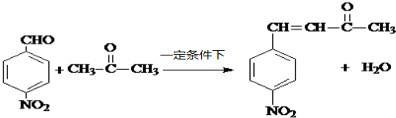 ��
��
��5��EΪ ��a���ں˴Ź������������������շ壬�ʴ��� b��E�к���̼̼˫�����ʻ���������D�к���ȩ����������̼̼˫����ȩ�����ܱ����Ը��������Һ���������Բ����������Ը��������Һ�� ��D��E���ʴ��� c��E�к���̼̼˫�����ʻ������������������Է����ӳɷ�Ӧ���ۺϷ�Ӧ��������Ӧ�ͻ�ԭ��Ӧ������ȷ�� d��̼̼˫��̼ԭ�����Ӳ�ͬ��֧�������Դ���˳���칹������ȷ��
��a���ں˴Ź������������������շ壬�ʴ��� b��E�к���̼̼˫�����ʻ���������D�к���ȩ����������̼̼˫����ȩ�����ܱ����Ը��������Һ���������Բ����������Ը��������Һ�� ��D��E���ʴ��� c��E�к���̼̼˫�����ʻ������������������Է����ӳɷ�Ӧ���ۺϷ�Ӧ��������Ӧ�ͻ�ԭ��Ӧ������ȷ�� d��̼̼˫��̼ԭ�����Ӳ�ͬ��֧�������Դ���˳���칹������ȷ��
��6��G�ṹ��ʽΪ ��
��
��7��GΪ �����ӽṹ��ֻ����һ������G��ͬ���칹����������������������Ȼ�����Һ������ɫ��Ӧ��˵�����з��ǻ���������̼��������Һ��Ӧ���ɶ�����̼���壬˵�������Ȼ��� ���ȡ����Ϊ-COOH��-C��CH��-OH�� ���-COOH��-OHλ����λ����4��ͬ���칹�壻 ���-COOH��-OHλ�ڼ�λ����3��ͬ���칹�壻 ���-COOH��-OHλ�ڶ�λ����3��ͬ���칹�壻 ���ȡ����Ϊ-C��CCOOH��-OH�����ڼ�����ֽṹ�� ������13��ͬ���칹�壻�ұ����ϵ�һ�ȴ���ֻ�����ֵ�ͬ���칹��Ľṹ��ʽΪ
�����ӽṹ��ֻ����һ������G��ͬ���칹����������������������Ȼ�����Һ������ɫ��Ӧ��˵�����з��ǻ���������̼��������Һ��Ӧ���ɶ�����̼���壬˵�������Ȼ��� ���ȡ����Ϊ-COOH��-C��CH��-OH�� ���-COOH��-OHλ����λ����4��ͬ���칹�壻 ���-COOH��-OHλ�ڼ�λ����3��ͬ���칹�壻 ���-COOH��-OHλ�ڶ�λ����3��ͬ���칹�壻 ���ȡ����Ϊ-C��CCOOH��-OH�����ڼ�����ֽṹ�� ������13��ͬ���칹�壻�ұ����ϵ�һ�ȴ���ֻ�����ֵ�ͬ���칹��Ľṹ��ʽΪ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¿����������ӣ�Na+��NH4+��Mg2+��Al3+��SO42����NO3����Cl����ijͬѧ�ռ��˸õ���������������Ҫ��Ԥ������������Һ����Ʋ���������µ�ʵ�飺

��֪��3NO3��+ 8Al + 5OH�� + 2H2O![]() 3NH3 + 8AlO2��
3NH3 + 8AlO2��
�������ϵ�ʵ�����������ͬѧ�ó��Ľ��۲���ȷ����
A�������п϶�����NH4+��Mg2+��SO42����NO3��
B��������һ������Al3+
C�������п��ܴ���Na+��Cl��
D���������п��ܴ���NaNO3��NH4Cl��MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ���������800��ʱ��Ӧ2NO(g)��O2(g)![]() 2NO2(g)��ϵ����n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ����n(NO)��ʱ��ı仯�����
![]()
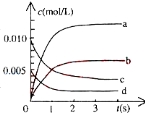
(1)д���÷�Ӧ��ƽ�ⳣ������ʽ��K��___________________����֪��K(300��)��K(350��)���÷�Ӧ��________�ȷ�Ӧ��
(2)��ͼ�б�ʾNO2�ı仯��������_______����O2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v��_________��
(3)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����__________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��������CuO��NH3��Ӧ���о�NH3��ij�����ʲ��ⶨ����ɣ����������ʵ��װ��(�г�װ��δ����)����ʵ�顣��ش��������⡣
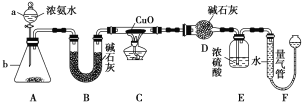
��1������a������Ϊ________������b�п�ѡ����Լ�Ϊ__________��
��2��ʵ�����У�����װ��A��������ȡ����ɫ������________(����ĸ)��
A��Cl2 B��O2 C��CO2 D��NO2
��3��ʵ���й۲쵽װ��C�к�ɫCuO��ĩ��Ϊ��ɫ���壬������������ɫ��ζ�������������������֤��NH3����________�ԣ�д����Ӧ�Ļ�ѧ����_ ��
��4��װ��E��Ũ�����������_______________________��
��5����ȡ�������ǰ��Ӧ��װ��F���еIJ�����________________________��
��6��ʵ����ϣ�����ø����D����m g��װ��F�����������Ϊn L(������ɱ�״��)�������е������ԭ�Ӹ�����ֵΪ________(�ú�m��n��ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����еĹ������ʣ�ֻ���ˮ�Ϳ��Լ����һ����
A. CaCO3��BaSO4��Na2CO3 B. CuSO4��NaCl��NaCO3
C. NaCl��CuSO4��CaCO3 D. NaCl��KNO3��BaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֶ�����Ԫ����ɵ�A��B��C��D��������ӣ�������18�����ӣ����Ƿ���������ԭ�ӵ���Ŀ����Ϊ2��3��4��6��A��C�����е�ԭ�Ӹ�����Ϊ1��1��B��D�����е�ԭ�Ӹ�����Ϊ1��2��D����Ϊ����ƽ�����ȼ�ϣ���ش��������⣺
��1��A��B��C��D���������ԭ�������ϴ������Ԫ�ص�һ�������ɴ�С���е�˳��Ϊ ����Ԫ�ط��Żش𣩣�
��2��A��HF��ȣ����ۡ��е�ϵͣ�ԭ���� ��
��3��B���ӵĿռ乹��Ϊ �Σ��÷������� ���ӣ�������ԡ��Ǽ��ԡ���
��4��CΪһ����ɫ���������й㷺Ӧ�ã���д��Cu��ϡH2SO4��C��Ӧ�Ʊ�����ͭ�����ӷ���ʽ: ���÷�Ӧ�з�Ӧ��Cuԭ�ӵĻ� ̬�����Ų�ʽΪ ��ͭ������ͭԭ�ӵĶѻ���ʽΪ���������ѻ�����ͼ��ͭ����һ��������ʾ��ͼ�����к� ��ͭԭ�ӣ�
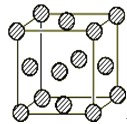
��5��D��������ԭ�ӵ��ӻ���ʽ�� ���ɸ�ԭ����ɵĵ��ʷ����а��� ���м�����õ��ʷ��ӻ�Ϊ�ȵ�����ij������ӵķ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ������ ��
A��1 mol H2��ռ���ԼΪ22.4 L
B��22 g CO2�к��е�������ԼΪ6.02��1023
C��100 mL 0.5 mol/L NaOH��Һ�к�����������Ϊ0.05 g
D����״���£�11.2 L O2��H2�Ļ����������������ԼΪ3.01��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M�ǵ�������Ԫ�أ������ֻ��1�����ӣ�����������ԭ�ӹ�����������ӡ�Ԫ��Y�ĸ�һ�����ӵ��������������������ͬ���ش��������⣺
��1������M�ľ�������Ϊ______��������ԭ�Ӽ�ͨ��_____�����γ����������ܶѻ�������Mԭ�ӵ���λ��Ϊ______��
��2��Ԫ��Y��̬ԭ�ӵĺ�������Ų�ʽΪ________����ͬ����Ԫ���У���һ������������______��дԪ�ط��ţ���Ԫ��Y�ĺ������У�������ǿ����________��д��ѧʽ������������ӵ����幹��Ϊ________��
��3��M��Y�γɵ�һ�ֻ����������������ͼ��ʾ��
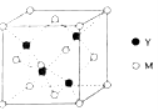
�ٸû�����Ļ�ѧʽΪ_______����֪��������a=0.542 nm���˾�����ܶ�Ϊ_______g��cm�C3����д������ʽ����Ҫ��������������ӵ�����ΪNA��
�ڸû�����������ˮ�������ڰ�ˮ����ԭ����________���˻�����İ�ˮ��Һ��������������Ϊ����ɫ������ɫ��Һ�������ӵĻ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
��1�� ��ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
![]()
һ���¶��£���һ���ݻ��̶����ܱ������У�����������Ӧ�����в����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����_______ (����ĸ)��
a�������е�ѹǿ����
b��1 mol H-H�����ѵ�ͬʱ����2 mol H-O��
c��������CO��=������H2��
d��c (CO) = c (H2) e���ԣ�H2O�����ԣ�CO�����ԣ�H2��=1:1:1
��2�� ����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�Ӧ
CO(g)+H2O(g) CO2 (g)+H2 (g) ���õ������������ݣ�
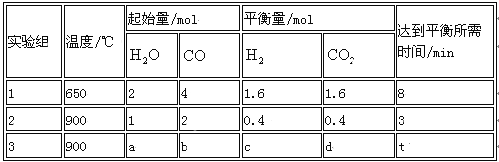
�� ʵ��1�дӿ�ʼ����ƽ��ʱCO��ʾ��Ӧ��ƽ������Ϊ mol/(l��min)��CO��g����ת����Ϊ ��
�� ʵ��2��H2O��g����ת����Ϊ ���÷�Ӧ���淴ӦΪ_______ (������š�)�ȷ�Ӧ��
�� ��ʵ��3ƽ��ʱҪ�ﵽ��ʵ��2��ƽ��ʱ�����ʵ����������ֱ���ȣ���t<3min����a��bӦ����Ĺ�ϵ ��______________ (�ú�a��b����ѧʽ��ʾ)��
��3��Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2 (g)+3H2 (g) CH3OH(g)+H2O(g)ͼ��1����ʾ�÷�Ӧ���й���������(��λΪkJmol-1��)�ı仯��
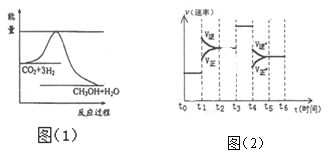
�� �����Ϊ1 L�ĺ����ܱ������У�����l molCO2��3molH2�����д�ʩ����ʹ c (CH3OH)�������_______ (����ĸ)
a�������¶�
b������He (g)��ʹ��ϵѹǿ����
c����H2O(g)����ϵ�з������
d���ٳ���l mol CO2��3 molH2
�� ����Ӧ�ﵽƽ��ʱ���ϸı�һ������(�����ı��������ʵ�����״̬)��Ӧ������ʱ��ı仯��ͼ��2���� ���б�ʾƽ��������CH3OH������ߵ�һ��ʱ����_______ ��t1��t2�ı������Ϊ ��t0��t1ƽ�ⳣ��ΪK1, t2��t3ƽ�ⳣ��ΪK2 ����K1 _______K2 (���������=������)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com