
| A、①② | B、①③ | C、②③ | D、①②③ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯碱工业中,通过电解饱和食盐水获得重要的化工原料,其产物中的氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、聚氯乙烯、氯苯等.
氯碱工业中,通过电解饱和食盐水获得重要的化工原料,其产物中的氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、聚氯乙烯、氯苯等.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X肯定为碱金属元素 |
| B、稳定性:Y的氢化物>Z的氢化物 |
| C、X、Y两元素形成的化合物可能为离子晶体 |
| D、Y、Z两元素形成的化合物熔点较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第七周期排满时有32种元素,全部是放射性元素 |
| B、第七周期排满时最后一种单质不与任何物质发生化学反应 |
| C、第七周期第ⅦA族元素的原子序数为117,是一种金属 |
| D、第七周期第ⅢA族元素的氢氧化物与Al(OH)3具有相似的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
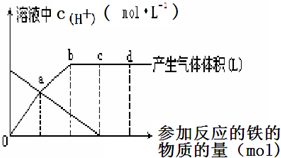 铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )
铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )| A、0点到a点的还原产物是NO |
| B、因反应放热,使溶液温度升高,a点到b点的还原产物是N2O |
| C、反应过程到达b点时HNO3已完全反应 |
| D、c点和d点参加反应的铁的物质的量之比是2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com