
����Ŀ��ijѧ����Na2SO3��AgNO3�ڲ�ͬpH�µķ�Ӧ����̽������������:
��1������pH��ʵ���¼����:
ʵ�� | pH | ���� |
a | 10 | ������ɫ����,�Ժ��ܽ�,��Һ���� |
b | 6 | ������ɫ������һ��ʱ�����δ�ܽ� |
c | 2 | ����������ɫ������һ��ʱ���������״�غ�ɫ����X |
�������ϵ�֪:
I.Ag2SO3:��ɫ,������ˮ,���ڹ���Na2SO3����Һ
II.Ag2O:�غ�ɫ,������ˮ���ܺ��ᷴӦ
���Ʋ�a�а�ɫ����ΪAg2SO3,���ӷ���ʽ��____________________________��
���Ʋ�a�а�ɫ����ΪAg2SO4,�Ʋ��������_________________________________��
��2��ȡb��c�а�ɫ����������Na2SO3��Һ�У������ܽ⡣��ͬѧ���ʵ��ȷ���˰�ɫ��������Ag2SO4,ʵ�鷽����:��ȡAg2SO4��������_________��Һ��,δ�ܽ⡣
��3����X����Һ���˳���ϴ����Ϊȷ������ɣ�ʵ������:
I.��X�еμ�ϡ���ᣬ�����Ա仯
II.��X�м������ŨHNO3,��������ɫ����
III.��Ba(NO3)2��Һ��BaCl2��Һ����II�з�Ӧ�����Һ��ǰ���ޱ仯�����߲�����ɫ����
��ʵ��I��Ŀ����_________________________��
�ڸ�������������X�����ʺ�Ԫ�������__________________________��
��II�з�Ӧ�Ļ�ѧ����ʽ��________________________��
��4����ͬѧ�ۺ�����ʵ�飬��������X��ԭ��,��Ϊ�������Ե���ǿ��SO32-��ԭ����ǿ����ͨ����һ��ʵ��ȷ�������ֿ����ԣ�ʵ��װ����ͼ��ʾ:

������Y��__________________��
�ڰ�ɫ����ת��ΪX�Ļ�ѧ����ʽ��__________________________��
���𰸡� 2Ag++SO32-=Ag2SO3�� SO32-�л�ԭ�ԣ���������ΪSO42-,������Ag+�������Ag2SO4���� ����Na2SO3 �ж�X������Ag2O �л�ԭ�ԣ�����AgԪ�أ�����SԪ�� Ag+2HNO3(Ũ)=AgNO3+NO2��+H2O SO2 Ag2SO3+ H2O![]() 2Ag+H2SO4
2Ag+H2SO4
����������1�����Ʋ�a�а�ɫ����ΪAg2SO3, Ag+��SO32-��Ӧ����Ag2SO3, Ag2SO3���ڹ����� Na2SO3��Һ,���ɳ��������ӷ���ʽΪ: 2Ag++SO32-=Ag2SO3������ȷ��: 2Ag++SO32-=Ag2SO3����
���Ʋ�a�а�ɫ����ΪAg2SO4�������ΪSO32-�л�ԭ��,���ܱ�����ΪSO42-,��Ag+��Ӧ���� Ag2SO4��ɫ��������ȷ����SO32-�л�ԭ�ԣ���������ΪSO42-��������Ag+�������Ag2SO4������
��2��Ag2SO3��ɫ��������ˮ�����ڹ���Na2SO3��Һ��ȡB��C�а�ɫ����������Na2SO3��Һ��,�����ܽ�,˵��B��C�а�ɫ����ΪAg2SO3����ȡAg2SO4����,ͬ�������������� Na2SO3��Һ��,���ж�������,���ֳ������ܽ�����ȷ��: ����Na2SO3��
��3�����������ܺ��������ɰ�ɫ�Ȼ���������ˮ, ��Һ��pH=2������������ɫ������һ��ʱ�������������״�غ�ɫ����X����X�еμ�ϡ�����������Ա仯��˵��X����Ag2O����ȷ��:����X�Ƿ�ΪAg2O ��
����X�м������ŨHNO3����������ɫ����ΪNO2��X��Ũ���ᷢ��������ԭ��Ӧ��X���л�ԭ����Xֻ��Ϊ����������ֻ��Ϊ�������X�к���AgԪ��������SԪ������ȷ��:�л�ԭ���� ����AgԪ��������SԪ����
����X�м������HNO3(Ũ)����������ɫ����ΪNO2���������ᷴӦ����Ԫ�ش�+5��Ϊ+4����ͬʱ������������ˮ����Ӧ����ʽΪ: Ag+2HNO3(Ũ)=AgNO3+NO2��+H2O����ȷ����Ag+2HNO3(Ũ)=AgNO3+NO2��+H2O��
��4��������״�غ�ɫ����XΪAg���������Ե���ǿ��+4����Ļ�ԭ����ǿ,�ܱ�+1������������ͨ��+4���������������������ʵ��ȷ����ͨ������������ƿ�а�ɫ����Ag2SO3ת��Ϊ�غ�ɫAg����ȷ����: SO2��
��XΪAg,��ɫ����ת��ΪAg,������������,����������+4�۵���,��+1��������������������,��ӦΪ: Ag2SO3+ H2O![]() 2Ag+H2SO4����ȷ����Ag2SO3+ H2O
2Ag+H2SO4����ȷ����Ag2SO3+ H2O![]() 2Ag+H2SO4��
2Ag+H2SO4��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���й����ʵĵ���ƽ�ⳣ�����£�
��ѧʽ | CH3COOH | H2CO3 | H2SO3 |
����ƽ�ⳣ�� | K=1.8��10��5 | K1=4.3��10��7 K2=5.6��10��11 | K1=1.5��10��2 K2=1.02��10��7 |
(1)��д��H2SO3�ĵ���ƽ�ⳣ��K1�ı���ʽ��________________��
(2) �����£������Ϊ10mL pH=2�Ĵ�����Һ����������Һ�ֱ������ˮϡ����1000mL��ϡ�ͺ���Һ��pH��ǰ��_____���ߣ����������������=������
(3)һ�������£��������ˮϡ��������Һ��������I���ˮ���V�仯��������ͼ��ʾ����a��b��c������Һ����ĵ���̶��ɴ�СΪ____________________��

(4)��������CH3COO����CO32����HSO3����SO32������Һ�н��H���������ɴ�С�Ĺ�ϵΪ___________��
(5)�����ͬ��c(H��)��ͬ�Ģ�CH3COOH����HCl����H2SO4 ��������Һ�ֱ���ͬŨ�ȵ�NaOH��Һ��ȫ�к�ʱ������NaOH��Һ������ɴ�С������˳����_____(�����)��
(6)��֪��H��(aq) + OH��(aq) == H2O(l) ��H =��57.3 kJ/mol��ʵ����ϡ������ϡNaOH��Һ��Ӧ����1 mol H2Oʱ�ų�57 kJ���ȣ��������Һ�У����������Ȼ�ѧ����ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)32 g CH4����Ħ������Ϊ_____��Լ����____mol���ӣ��ڱ�״������ռ�����ԼΪ___L��
(2)����������ʵ���Ũ�ȵ�Ca(OH)2��Һ��NaHCO3��Һ��ϣ����ӷ���ʽΪ��_____��
(3)H++HCO3-��H2O+CO2����Ӧ��һ����ѧ����ʽ_______________________��
(4)�Ʊ�����������������ӷ���ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�±�Ϊ25��ʱijЩ����ĵ���ƽ�ⳣ��������������Ϣ�жϣ�����˵����ȷ����
CH3COOH | HClO | H2CO3 |
Ka=1.8��10-5 | Ka=3.0��10-8 | Ka1=4.4��10-7 Ka2=4.7��10-11 |
A. ��NaClO��Һ��ͨ������������̼�����ӷ���ʽΪ��2ClO-+CO2+H2O=2HClO+CO32-
B. ��ͬŨ�ȵ�CH3COONa��NaClO�Ļ����Һ�У�c(CH3COOH)+c(HClO)��c(OH-)-c(H+)
C. 25��ʱ��0.10mol��L-1Na2CO3��Һͨ��CO2����Һ��pH=7ʱ,��Һ�У�c(Na+)=c(CO32-)+ c (HCO3-)+c(H2CO3)
D. ��0.1mol��L-1CH3COONa��Һ�м�������ˮ����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ�Ǻϳ�ʳƷ���װ���Ͼ���ϩ�ĵ����������ɶ����ѽ��Ʊ����ѽ�ĸ���ӦΪC4H10(g,������) ![]() CH4(g)+C3H6(g)
CH4(g)+C3H6(g)
��ش���������
��1����ѧ�ϣ����ȶ����ʵ�������Ϊ0����Ԫ�صĵ��ʻ��ϳɵ�һ������ʱ�ķ�Ӧ�Ƚиû�����������ȣ������ȿɱ�ʾ���������������25�桢101kPa�����л�������������±���ʾ:
���� | ���� | ���� | ��ϩ | ��ϩ | ������ | �춡�� |
������/ kJ��mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
���������ѽ�������ϩ���Ȼ�ѧ����ʽΪ_______________________________��
��2��һ���¶������ں����ܱ�������Ͷ��һ���������鷢����Ӧ������ϩ��
�����������˵���÷�Ӧ�ﵽƽ��״̬����__________(����)
A.�����ܶȱ��ֲ��� B.c(C2H4)��c(C2H6)/c(C4H10)���ֲ���
C.��Ӧ�ȱ��ֲ��� D.������ֽ����������������������
��Ϊ����߷�Ӧ���ʺͷ�Ӧ���ת�������ɲ��յĴ�ʩ��______________________________��
��3�����ܱ������г��������飬��һ������(Ũ�ȡ�������ѹǿ��)�·�����Ӧ�������ϩ�������¶ȹ�ϵ��ͼ��ʾ���¶ȸ���600��ʱ�������¶���������ϩ���ʽ��ͣ����ܵ�ԭ����____________________________________________��

��4����һ���¶�����10L�����ܱ������г���2mol�����飬��Ӧ������ϩ������������10min�ﵽƽ��״̬�����ƽ��ʱ����ѹǿ��ԭ����1.75����
��0~10min���������������v(C2H6)=__________ mol��L-1��min-1
�����������£��������ƽ��ת����Ϊ______________���÷�Ӧ��ƽ�ⳣ��KΪ____________�� (5)����һ����ȼ�ϵ�������ڵ�K2CO3(���в���O2-��HCO3-)Ϊ��������Ծ��д����ú͵������ܵ�ϡ����������Ϊ�缫����ȼ�ϵ�ص�������ӦʽΪ26CO2+13O2+52e-=26CO32-������ӦʽΪ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ijѧ����0.1500 mol/L NaOH��Һ�ⶨijδ֪Ũ�ȵ�������Һ��������ɷֽ�Ϊ���¼�����
A��������ˮϴ���ζ���
B���ô��ⶨ����Һ��ϴ��ʽ�ζ���
C������ʽ�ζ���ȡϡ����25.00 mL��ע����ƿ�У������̪
D����ȡ��ƿ�����ظ�����2��3��
E�����ζ����Ƿ�©ˮ
F��ȡ�¼�ʽ�ζ����ñ�NaOH��Һ��ϴ����Һע���ʽ�ζ��ܡ�0���̶�����2��3 cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ������0���̶Ȼ�0���̶�����
G������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶�
���������գ�
��1���ζ�ʱ��ȷ������˳���ǣ��������ĸ��д����____�� �� F �� �� �� �� D��
��2������F��Ӧ��ѡ��ͼ�еζ���_____�����ţ���

��3���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧע��۲�_____��
��4���ζ���������ʾ��
�ζ����� | ����Һ���/mL | ����Һ�����/mL | |
�ζ�ǰ�̶� | �ζ���̶� | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 0.60 | 20.60 |
3 | 25.00 | 0.20 | 20.19 |
�������������ʵ���Ũ��Ϊ_____����ȷ��0.0001����
��5�����в����ᵼ�²ⶨ���ƫ�ߵ���_____��
A����ʽ�ζ�����װҺǰδ�ñ�NaOH��Һ��ϴ
B���ζ������У���ƿҡ����̫���ң���ƿ����Һ�ν���
C����ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ��յ�ʱ��������
D���ﵽ�ζ��յ�ʱ�����Ӷ���
��6��������ԭ�ζ�ʵ��������к͵ζ����ƣ�����֪Ũ�ȵ���������Һ�ζ�δ֪Ũ�ȵĻ�ԭ����Һ��֮������Ѫ�Ƶĺ���ʱ����������ʵ�飺
�ٿɽ�2mLѪҺ������ˮϡ�ͺ������м�����������泥�NH4��2C2O4���壬��Ӧ���� CaC2O4��������������ϡ���ᴦ����H2C2O4��Һ��
�ڽ��ٵõ���H2C2O4��Һ����������KMnO4��Һ�ζ�����������ΪCO2����ԭ����ΪMn2+��
���յ�ʱ��ȥ20mL l.0��l0��4 mol/L��KMnO4��Һ��
��д����KMn04�ζ�H2C2O4�����ӷ���ʽ_____________________��
���жϵζ��յ�ķ�����________________________��
���㣺ѪҺ�к������ӵ�Ũ��Ϊ_____mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���Ϊͬ����������ǣ� ��
A.�ɱ��ͱ�B.���ͺ���C.���������D.����Ͷ�ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ֶ����ڽ���Ԫ�غ�һ�ַǽ���Ԫ����ɵĻ�����X����ˮ�������ֽⷴӦ��ijУ��ȤС������ͼװ��(�г�װ����ȥ)�������̽��ʵ�顣
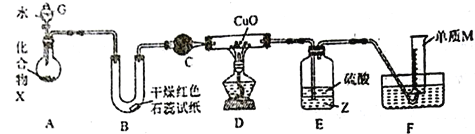
(1)����G��������_____________________��B�к�ɫʯ����ֽ����������M�ĵ���ʽΪ___________________��
(2)������X�к���ɵ���M��Ԫ����������Ϊ16.9%��д��X��ˮ��Ӧ�Ļ�ѧ����ʽ��_____________________________��
(3)C�е��Լ�����Ϊ___________________________��
(4)ʵ��ʱ��װ��D��Ӳ�ʲ������ڵ�����Ϊ_________________________��
(5)�b��E���Լ�ZΪ___________(�ѧʽ)��װ��E��������_________________________��
(6)����ͨ��E��F��װ�ã������ʵ�鷽��֤��D�з����˷�Ӧ(��ͨ���۲�D�й�����ɫ�����仯)��__________________________________________________��
(7)��װ��A�й�����Ʒ��������(���ʲ����뷴Ӧ)��ijͬѧͨ���ⶨF�е���M�ڱ�״���µ����������Ʒ����������ȷ��������Ʒ��X�������������жϸ÷����Ƿ���У���˵��ԭ��__________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȩ�����ﱨ����1996���ѧ���������з���H3���ӡ��ס��ҡ���������λѧ���Դ˱�������ʶ��ȷ����
A������Ϊ�������־��Բ����ܣ���ΪH3����Υ���˹��ۼ�����
B������Ϊ�����л����ܴ�����һ���ⵥ�ʣ���Ϊ��Ԫ��������ͬλ�ر�Ȼ������ͬ��������
C������ΪH3����ʵ������H2������H��������ۼ���ϵIJ��Ӧд��H
D������Ϊ��������ķ��ִ��ڣ���֤����ͳ�ļۼ�������һ���ľ������д�������չ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com