
有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
| A.N2O与SiO2为等电子体、具有相似的结构(包括电子式) |
B.N2O的电子式可表示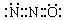 |
| C.N2O与CO2均不含非极性键 |
| D.N2O为三角形分子 |
科目:高中化学 来源: 题型:单选题
砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是
| A.分子中共价键键角均为109°28′ | B.黄砷中共价键键能大于白磷 |
| C.黄砷分子极性大于白磷 | D.黄砷的熔点高于白磷 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫的卤化物(S2X2)是广泛用于橡胶工业的硫化剂,S2C12分子结构如图所示。遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )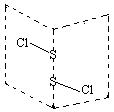
| A.稳定性S2C12>S2Br2 |
| B.反应中,生成1molSO2,转移电子为3mol |
| C.分子中同时含有极性键和非极性键且各原子都满足8电子稳定结构 |
| D.因为S-Cl键能比S-Br键能大,S2C12沸点比S2Br2高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法中,不正确的是( )
| A.离子晶体的晶格能越大,离子晶体的熔点越高 |
| B.碘单质在水中溶解度很小,但在CCl4中溶解度很大,这是因为CCl4和I2都是非极性分子,而H2O是极性分子 |
| C.成键原子的原子轨道重叠越多,共价键越牢固 |
| D.含有金属阳离子的晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对P4S3分子的结构研究表明,该分子中不存在不饱和键,且各原子最外层均已达到8个电子稳定结构。则一个P4S3分子中含有的共价键个数为
| A.7个 | B.9个 | C.19个 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
| A.①③⑤ | B.②④⑤ | C.②③④ | D.①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是
| A.浓氨水 | B.NaOH溶液 | C.CCl4 | D.AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于含正离子N5+的化合物N5ASF6,下列叙述中错误的是( )
| A.N5+共有34个核外电子 |
| B.N5+中氮原子间以离子键结合 |
| C.化合物N5ASF6中AS的化合价为+1价 |
| D.化合物N5ASF6为离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com