
【09届广州天河区高三二模化学】一些烷烃的燃烧热如下表:
| 化合物 | 燃烧热/kJ·mol-1 | 化合物 | 燃烧热/kJ·mol-1 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
下列表达正确的是
A. 正戊烷的燃烧热小于3531.3kJ·mol-1
B. 稳定性:正丁烷<异丁烷
C. 乙烷燃烧的热化学方程式为:
2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ;△H= -1560.8 kJ·mol-1
D. 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 操作 | 现象 | 结论 | |
| 步骤一 | 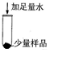 |
固体部分溶解 固体部分溶解 |
猜想二成立 |
| 步骤二 | 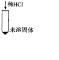 |
固体溶解,产生气泡 固体溶解,产生气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
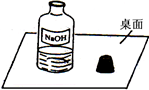 (2013?天河区一模)一天,小明走进实验室,看到了一幅“不和谐”的画面(如图).围绕此瓶试剂是否变质的问题,展开了探究.
(2013?天河区一模)一天,小明走进实验室,看到了一幅“不和谐”的画面(如图).围绕此瓶试剂是否变质的问题,展开了探究.| 实验步骤 | 预期现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 2C
2C 2C
2C| c2(C) |
| c(A)?c2(B) |
| c2(C) |
| c(A)?c2(B) |
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
(2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH-
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com