
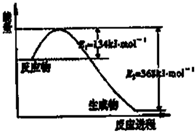
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,| t(s) | 0 | 500 | 1000 | 1500 |
| N(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
| c2(N2O5) |
| c4(NO2)?c(O2) |
| c2(N2O5) |
| c4(NO2)?c(O2) |


科目:高中化学 来源: 题型:
| A、X一定大于Y |
| B、X可能等于Y |
| C、X可能小于Y |
| D、X可能大于Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混和液中c(Cl-)=c(Na+) |
| B、混和液中c(Cl-)=2c(SO42-) |
| C、混和前两溶液体积相等 |
| D、混和前两溶液中MgCl2与Na2SO4物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
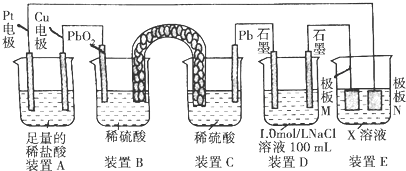
 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某反应2A (g)+B(g)═3C(s)在室温下可自发进行,则该反应的△H<0 | ||
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | ||
C、CH3COOH 溶液加水稀释后,溶液中
| ||
| D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH 减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| B、分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 |
| C、加热氯化钠溶液得氯化钠固体,需用表面皿 |
| D、从氯酸钾和二氧化锰制氧气后的混合物中分离出可溶物的操作步骤:溶解→过滤→蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
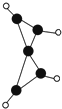 科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )| A、充分燃烧等质量的X和甲烷,X消耗氧气较多 |
| B、X是一种常温下能稳定存在的液态烃 |
| C、X和乙烷类似,都容易发生取代反应 |
| D、X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com