
| A、某反应2A (g)+B(g)═3C(s)在室温下可自发进行,则该反应的△H<0 | ||
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | ||
C、CH3COOH 溶液加水稀释后,溶液中
| ||
| D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH 减小 |
| c(CH3COOH) |
| c(CH3COO-) |


科目:高中化学 来源: 题型:
| A、4.32 g |
| B、4.68 g |
| C、5.36 g |
| D、6.38 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 放出,如图中符合这一情况的是( )
放出,如图中符合这一情况的是( )| A极板 | B极板 | X电极 | Z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
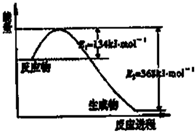 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,| t(s) | 0 | 500 | 1000 | 1500 |
| N(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量时,将固体NaOH直接放在天平左盘上 |
| B、将烧杯中溶解固体NaOH所得溶液,立即转移至500ml容量瓶中 |
| C、配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果 |
| D、缓缓地将蒸馏水注入500ml容量瓶至溶液的凹液面正好与刻度线相切 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速率变化时,化学平衡一定发生移动 |
| B、化学平衡发生移动时、化学反应速率一定变化 |
| C、正反应进行的程度大、正反应速率一定大 |
| D、只有使用催化剂才会发生化学反应速率变化,而化学平衡不移动的情况. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com