
【题目】元素周期表中的四种元素的有关信息如下,请用合理的化学用语填写空白。
在周期表中的区域 | 元素代号 | 有关信息 |
短周期元素 | X | X的最高价氧化物的水化物甲是一种胃酸中和剂,且能溶于强碱溶液 |
Y | Y的一种氢化物可用于制造纯碱和做制冷剂 | |
长周期元素 | Z | Z的一种盐乙可以作净水剂,Z的某种氧化物丙可以做红色涂料 |
W | W元素大多存在于海藻种,它的银盐可用于人工降雨 |
(1)X元素周期表中的位置为___,X、Y、Z三种元素的简单离子半径从大到小的顺序为___。
(2)足量W的最高价氧化物的水化物是稀溶液与1mol甲完全反应,放出热量QkJ,请写出表示该过程中和热的热化学方程式:____。
(3)下列有关W的气态氢化物丁的说法正确的有___(选填字母)
a.丁比氯化氢沸点高 b.丁比氯化氢稳定性好
c.丁比氟化氢还原性弱 d.丁比氟化氢酸性弱
(4)请写出丙溶于丁的水溶液的离子方程式___。
【答案】第三周期ⅢA族 r(Fe3+)>r(N3-)>r(Al3+) HIO4(aq)+![]() Al(OH)3(s)=H2O(l)+
Al(OH)3(s)=H2O(l)+![]() Al(IO4)3(aq) △H=-
Al(IO4)3(aq) △H=-![]() QkJ/mol a Fe2O3+6H++2I-=2Fe2++I2+3H2O
QkJ/mol a Fe2O3+6H++2I-=2Fe2++I2+3H2O
【解析】
氢氧化铝具有两性,X的最高价氧化物的水化物甲是一种胃酸中和剂,且能溶于强碱溶液,X是Al元素;氨气作制冷剂,Y的一种氢化物可用于制造纯碱和做制冷剂,Y是N元素; 氧化铁是红色染料的成分,Z的一种盐乙可以作净水剂,Z的某种氧化物丙可以做红色涂料,Z是Fe元素;碘化银用于人工降雨,W元素大多存在于海藻种,它的银盐可用于人工降雨,W是I元素;
(1)X是Al元素,Al元素周期表中的位置为第三周期ⅢA族,电子层数越多半径越大,电子层数相同,质子数越多半径越小,Al3+、N3-、Fe3+三种离子半径从大到小的顺序为r(Fe3+)>r(N3-)>r(Al3+)。
(2)W的最高价氧化物的水化物是HIO4,甲是氢氧化铝;足量HIO4稀溶液与1mol Al(OH)3完全反应,放出热量QkJ,表示该过程中和热的热化学方程式是HIO4(aq)+![]() Al(OH)3(s)=H2O(l)+
Al(OH)3(s)=H2O(l)+![]() Al(IO4)3(aq) △H=-
Al(IO4)3(aq) △H=-![]() QkJ/mol。
QkJ/mol。
(3)a.HI的相对分子质量大于HCl,HI比氯化氢沸点高,故a正确;
b. Cl的非金属性大于I ,HCl比HI稳定性好,故b错误;
c. Cl的非金属性大于I, HI比氟化氢还原性强,故c错误;
d. HI是强酸,氢氟酸是弱酸,故d错误。
(4)铁的氧化物丙可以做红色涂料,丙是Fe2O3,丁是HI,Fe2O3与HI发生氧化还原反应生成FeI2和I2,反应的离子方程式是Fe2O3+6H++2I-=2Fe2++I2+3H2O。


科目:高中化学 来源: 题型:
【题目】如图是某元素的价类二维图。其中X是一种强碱,G为正盐,通常条件下Z是无色液体,D的相对原子质量比C小16,各物质转化关系如图所示。下列说法正确的是
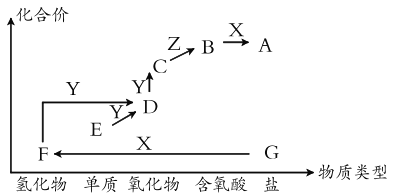
A.E 可以是金属也可以是非金属
B.C 和 D 两种大气污染物,都能用排空气法收集
C.B 的浓溶液具有吸水性,可用来干燥气体
D.实验室制备 F 时,可以将其浓溶液滴入碱石灰中进行制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10O2的有机物R在酸性条件下可水解为酸和醇,下列说法不正确的是
A.这些醇和酸重新组合可形成的酯共有40种
B.分子式与R相同的酸与足量碱石灰共热,最多可得到2种烷烃
C.R水解得到的酸至少有5对共用电子对数目
D.R水解得到的醇发生消去反应,可得到4种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义。
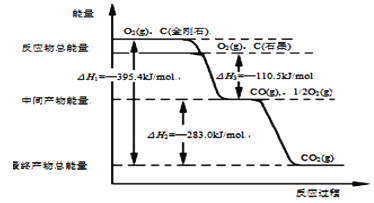
(1)金刚石和石墨燃烧反应中的能量变化如图所示。在通常状况下,金刚石和石墨中,__(填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为___。
(2)采用电化学法可将二氧化碳转化为甲烷,试写出以氢氧化钾水溶液作电解质溶液时,该转化的电极反应式为___。
(3)以CO2为原料还可以合成多种物质。工业上常以CO2(g)与H2(g)为原料合成乙醇。
①已知:H2O(l)=H2O(g) △H=+44kJ·mol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ·mol-1
CO2(g)+H2(g) △H=-41.2kJ·mol-1
2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-256.1kJ·mol-1
CH3CH2OH(g)+H2O(g) △H=-256.1kJ·mol-1
则:CO2气体与氢气反应生成气态乙醇和液态水的热化学方程式为___。
②如图是一种以烟道气为原料合成乙醇的工作原理示意图。对该流程的分析,下列说法正确的是___。

A.该流程至少包含4种形式的能量转化
B.装置X中为了增强水的导电性,通常向其中加入少量Na2SO4或NaOH
C.合成塔中生成乙醇的反应是化合反应
D.流程设计体现了绿色化学思想
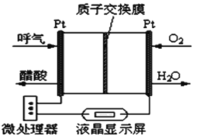
③如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池负极的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制成500mL 0.5mol/L的稀H2SO4
(1)填写下列操作步骤:
①所需浓H2SO4的体积为____。
②如果实验室有10mL、20mL、50mL量筒,应选用___mL量筒量取。
③将量取的浓H2SO4沿玻璃棒慢慢注入盛有约100mL水的___里,并不断搅拌,目的是___。
④立即将上述溶液沿玻璃棒注入____中,并用50mL蒸馏水洗涤烧杯2~3次,并将洗涤液注入其中,并不时轻轻振荡。
⑤加水至距刻度___处,改用__加水,使溶液的凹液面正好跟刻度相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误:____。
(3)误差(填偏高、偏低、无影响)
①操作②中量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将___;
②问题(2)的错误操作将导致所配制溶液的浓度___;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知MnO2为黑色难溶于水的固体,实验室制取氧气的反应为2KClO3![]() 2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
A. 溶解、过滤、蒸发、洗涤 B. 溶解、过滤、洗涤、加热
C. 溶解、蒸发、洗涤、过滤 D. 溶解、洗涤、过滤、加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.相同条件下,N2和O3混合气体与等体积的N2所含的原子数相同
B.等物质的量的CH5+和OH-所含电子数相等
C.常温常压下,28gCO与22.4LO2所含分子数相等
D.16gCH4与18gNH4+所含质子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有以下离子中的若干种:K+、Cl-、NH、Mg2+、CO![]() 、Ba2+、SO
、Ba2+、SO![]() 。现取3份该溶液各100 mL分别进行如下实验:
。现取3份该溶液各100 mL分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
① | 加AgNO3溶液 | 有白色沉淀生成 |
② | 加足量NaOH溶液并加热 | 收集到气体,在标准状况下体积为2.24 L |
③ | 加足量BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为12.54 g,第二次称量读数为4.66g |
试回答下列问题:
(1)根据实验①对Cl-是否存在的判断是_______________(填“一定存在”“一定不存在”或“不能确定”);根据实验①~③判断混合物中一定不存在的离子是___________。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
阴离子符号 | 物质的量浓度(mol/L) |
__________ | |
(3)试确定K+是否存在 __________ (填“是”或“否”),判断的理是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
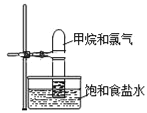
【题目】将如图装置放置在光亮的地方,随后观察到如下实验现象:大试管内壁上有油状液滴生成、饱和食盐水中有少量固体析出、黄绿色气体颜色变浅、试管内液面有所上升。
(1)油状液滴的成分可能是CCl4和___。
(2)水槽中盛放饱和食盐水而不是蒸馏水是为了抑制___与水的反应。
(3)试管内液面上升的原因是___极易溶于水。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com