
| Ⅰ | Ⅱ | Ⅲ | |
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 13.8g | 14.2g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、根据表中第Ⅱ组数据不能计算出混合物中NaHCO3的质量分数 |
| B、加入混合物9.2g时盐酸过量 |
| C、盐酸的物质的量浓度为3.0mol?L-1 |
| D、13.8g混合物恰好与盐酸完全反应 |
| n |
| V |
| 3.36L |
| 2.24L |
| 3.36L |
| 22.4L/mol |
| 0.15mol |
| 0.05L |
| 3.36L |
| 2.24L |


科目:高中化学 来源: 题型:
| A、18g 2H2O含有10NA个电子 |
| B、1mol苯含有6NA个C-H键 |
| C、常温常压下,22.4L NH3约含有NA个NH3分子 |
| D、27g铝片投入足量浓H2SO4中生成1.5NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 硝酸溶液总体积 | 100mL | 200mL | 300mL | 400mL | 500mL |
| 剩余固体的质量 | 18.6g | 9.6g | 0g | 0g | 0g |
| 气体体积 | 2.24L | 4.48L | 6.72L | 8.4L | 8.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、食盐可作氯碱工业的原料 |
| B、碘酒是指单质碘的乙醇溶液 |
| C、大量使用化肥和农药,以提高农作物产量,符合绿色化学的原则 |
| D、低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
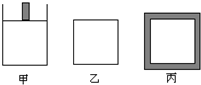 800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行.
800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热 |
| B、两者分别与同浓度的稀盐酸反应 |
| C、溶于水,比较其溶解性 |
| D、两者分别加入NaOH溶液或石灰水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com