
【题目】常温下,向10mL 0.1 mol·L-1的HR溶液中逐滴滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及导电能力变化如图。下列分析不正确的是
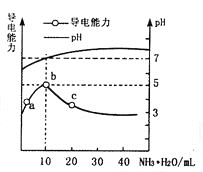
A. a~b点导电能力增强,说明HR为弱酸
B. b点溶液pH=5,此时酸碱恰好中和
C. c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
D. b、c两点水的电离程度:b<c
科目:高中化学 来源: 题型:
【题目】我国科学家发明的水溶液锂电池为电动汽车发展扫除了障碍,装置原理如下图所示,其中固体薄膜只允许Li+通过。锂离子电池的总反应为xLi +Li1-xMn2O4![]() LiMn2O4,下列有关说法错误的是
LiMn2O4,下列有关说法错误的是

A. 放电时,Li+穿过固体薄膜进入到水溶液电解质中
B. 放电时,正极反应为Li1-xMn2O4+xLi++xe-![]() LiMn2O4
LiMn2O4
C. 该电池的缺点是存在副反应:2Li +2H2O![]() 2LiOH+H2↑
2LiOH+H2↑
D. 充电时,电极b为阳极,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
下列离子方程式正确的是
A. Fe3O4溶于足量稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O
B. 4mol/LNaAlO2溶液与7mol/L盐酸等体积混合:4AlO2-+7H++H2O=3Al(OH)3↓+A13+
C. ![]() 与浓盐酸在加热条件下生成氯气:
与浓盐酸在加热条件下生成氯气:![]() +6Cl-+6H+=
+6Cl-+6H+=![]() 十3Cl2↑+3H2O
十3Cl2↑+3H2O
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同一主族从上到下,有关卤族元素的说法正确的是( )
A.原子半径逐渐增大
B.单质氧化性逐渐增强
C.气态氢化物的稳定性逐渐增强
D.都有最高价氧化物的水化物,化学式为HXO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列各组物质的分类正确的是
①混合物:水玻璃、水银、水煤气
②电解质:明矾、冰醋酸、石膏
③酸性氧化物:CO2、Al2O3、SO3
④同位素:1H、2H2、3H
⑤同素异形体: C60、金刚石、石墨
⑥干冰、液氯等都是非电解质
A. ①②③④⑤⑥ B. ④⑥ C. ②⑤⑥ D. ②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 二氧化硫溶于水能导电,故二氧化硫属于电解质
B. 硫酸钡难溶于水,故硫酸钡属于弱电解质
C. 硫酸是强电解质,故纯硫酸能导电
D. 氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 明矾净水原理是氢氧化铝胶粒能吸附水中杂质
B. 根据能否产生丁达尔效应将分散系分为胶体、溶液和浊液
C. 面粉厂、水泥厂“电泳除尘”是利用了胶体带电
D. 利用过滤操作可以提纯蛋白质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,11g CO2含有的共用电子对数为0.5NA
B. 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA
C. 通常状况下,39 g Na2O2固体中含有的离子总数为2NA
D. 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠(NaA)可作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2。已知25 ℃时,HA、H2CO3的电离平衡常数分别为 K=6.25×10-5、 K1=4.3×10-7,则下列说法正确的是(不考虑饮料中其他成分) ( )
A.提高CO2充气压力,饮料中c(A-)不变
B.当pH为5.0时,饮料中![]()
C.相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
D.结合H+的能力:A-> HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com