
����Ŀ����������(NaA)�������ϵķ��������о�����������(HA)���־�������������A����������̼�����ϵĹ����У���������NaA�⣬�����ѹ����CO2����֪25 ��ʱ��HA��H2CO3�ĵ���ƽ�ⳣ���ֱ�Ϊ K��6.25��10��5�� K1��4.3��10��7��������˵����ȷ����(�����������������ɷ�) �� ��
A�����CO2����ѹ����������c(A��)����
B����pHΪ5.0ʱ��������![]()
C�������δ��CO2�����ϣ�̼�����ϵ��־������ϵ�
D�����H+��������A��> HCO3��
���𰸡�B
��������
���������A�����CO2����ѹ������Һ��������ǿ����Һ��c��A-����С����A����B����pHΪ5.0ʱ��������c(HA)/c(A-)=c(H+)/Ka=10-5/(6.25��10-5)=0.16����B��ȷ��C����������Ϣ��֪�������ᣨHA�����־�������������A-����CO2��������HA��Ũ�Ƚϴ����������δ��CO2�����ϣ�̼�����ϵ��־������ϸߣ���C����D���������Խǿ���������ӽ����������Խ����HA������ǿ��H2CO3�����Խ��H+��������A-��HCO3-����D��������ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10mL 0.1 mol��L-1��HR��Һ����ε���0.1mol��L-1��NH3��H2O��Һ��������ҺpH�����������仯��ͼ�����з�������ȷ����
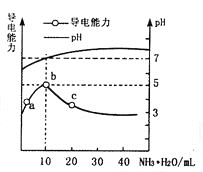
A. a��b�㵼��������ǿ��˵��HRΪ����
B. b����ҺpH=5����ʱ���ǡ���к�
C. c����Һ����c(NH4+)>c(R-)��c(OH-)>c(H+)
D. b��c����ˮ�ĵ���̶ȣ�b<c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ˮ�����������ά������Ҫ�Ļ���ԭ�ϡ����ǵĺϳ�·����ͼ��ʾ��
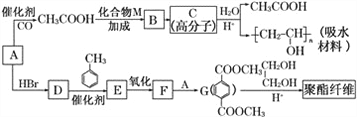
��֪����A��C��H��O����Ԫ����ɣ���Է�������Ϊ32��
��RCOOR�䣫R��OH![]() RCOOR�士R��OH(R��R�䡢R���������)��
RCOOR�士R��OH(R��R�䡢R���������)��
��ش��������⣺
��1�� A�Ľṹ��ʽ��____________________��
��2��B�еĹ�����������______________________��
��3��D��E�ķ�Ӧ������______________��
��4���������뻯����M��Ӧ�Ļ�ѧ����ʽ��_________________________________
��G��������ά�Ļ�ѧ����ʽ��______________��
��5�� E��������___________��
��6�� G��ͬ���칹���ж��֣��������������Ĺ���_____�֡�
�ٱ�����ֻ������ȡ������
�� 1 mol��������������NaHCO3��Һ��Ӧ����2 mol CO2��
(7) д����![]() �ϳ�
�ϳ�![]() ������ͼ(ע����Ӧ����)________��
������ͼ(ע����Ӧ����)________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��λ�ڶ����ڵ�����Ԫ�ء���֪�������ȶ��ԣ�HmD>HmC����Cm-��E(m-1)-
������ͬ�ĵ��Ӳ�ṹ����A��B��ͬһ���ڣ��ڸ�������������Ԫ���У�A��ԭ�Ӱ뾶���B�����Ӱ뾶��С����A��B������֮����D��������3��������������Ϣ����Ӧ�Ļ�ѧ����ش��������⣺
(1)HmDm�ĵ���ʽ__________��
(2)Cm-��E(m-1)-�Ļ�ԭ��ǿ��˳��Ϊ__________(�����ӷ��ű�ʾ)����֤���仹ԭ��ǿ�������ӷ���ʽΪ____________________��
(3)д��B������AԪ�ص�����������Ӧˮ�������Һ��Ӧ�����ӷ���ʽ___________________��
(4)�����ж�C��D�ǽ�����ǿ����������__________
A.��̬�⻯����ȶ��� B.�û���Ӧ C.�������������׳̶�
D.��ۺ���������� E.�õ�����Ŀ����
F.����������Ȼ��Ĵ�����ʽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���������ͬ�� Ba(OH)2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4�� NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ�����з�������ȷ���ǣ� ��
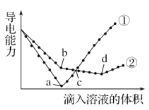
A���ٴ����μ�H2SO4��Һ�ı仯����
B��b�㣬ˮ���������c(H+)< 10��7 mol/L
C��c�㣬����Һ�к�����ͬ���� OH��
D��a��d�����Ӧ����Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����A��B��0.32 mol��������ܱ������У�������Ӧ��A(g)��B(g)![]() 2C(g) ��H=��a kJ��mol��1 (a>0)����Ӧ�����вⶨ���������±�������˵����ȷ���ǣ� ��
2C(g) ��H=��a kJ��mol��1 (a>0)����Ӧ�����вⶨ���������±�������˵����ȷ���ǣ� ��
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A������ʼʱ�������г���0.64 mol C�����ƽ��ʱ���յ�����Ϊ0.12a kJ
B�����£� ���ѹ�����������B��Ũ�Ⱥ��������������
C������ʼʱ�������г��� 0.64 mol A �� 0.64 mol B�� ���ƽ��ʱ n(C)<0.40 mol
D�����¡����ݣ���ƽ����ϵ���ٳ���0.32 mol A���ٴ�ƽ��ʱ��B��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�RO![]() ��R���ɷ�����Ӧ��RO
��R���ɷ�����Ӧ��RO![]() ��5R����6H��===3R2��3H2O�����й���RԪ�ص������У���ȷ����(����)
��5R����6H��===3R2��3H2O�����й���RԪ�ص������У���ȷ����(����)
A. R2�ڳ��³�ѹ��һ�������� B. RO![]() �е�Rֻ�ܱ���ԭ
�е�Rֻ�ܱ���ԭ
C. Ԫ��Rλ�����ڱ��еڢ�A�� D. ��1 mol RO![]() ����÷�Ӧ����ת�Ƶ��ӵ����ʵ���Ϊ5 mol
����÷�Ӧ����ת�Ƶ��ӵ����ʵ���Ϊ5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Zn(OH)2�����ڰ�ˮ����[Zn(NH3)4]2+: Zn(OH)2+4NH3��H2O=Zn(NH3)4]2++4H2O+2OH-
��1��ԭ��������ZnԪ��С1��Ԫ�ط���Ϊ____����Ԫ��ԭ�ӻ�̬��������Ų�ʽΪ______��
��2��NH3��H2O�ķе������ͬ��Ԫ���⻯��ķе㣬����Ϊ________��
��3��NH3��Nԭ�ӹ�����ӻ�������______��
��4����H2O���ӻ�Ϊ�ȵ�����ķ���Ϊ_____��
��5����п����һ����Ȼ�纬ZnԪ�صĿ���侧��ṹ�����������壨����ͼ��ʾ������������ZnS����ṹ��S2-����λ��Ϊ________��Zn2+�ķ�������Ϊ��l/4,l/4,l/4������3/4, 3/4,l/4������3/4��l/4,3/4������1/4,3/4,3/4������S2-�ķ�������Ϊ______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л���˵������ȷ����
A. CH3CH(OH)CH2COOHϵͳ����������3-�ǻ�����
B. �ı�����ϩ(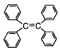 )������̼ԭ��һ������ͬһƽ��
)������̼ԭ��һ������ͬһƽ��
C. lmol 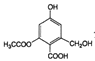 �ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ���3mol��4mol��1mol
�ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ���3mol��4mol��1mol
D. ��һ�������£�����Һ�塢Ũ���������屽���������ķ�Ӧ������ȡ����Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com