
【题目】在一定条件下,RO![]() 与R-可发生反应:RO
与R-可发生反应:RO![]() +5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
+5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
A. R2在常温常压下一定是气体 B. RO![]() 中的R只能被还原
中的R只能被还原
C. 元素R位于周期表中第ⅤA族 D. 若1 mol RO![]() 参与该反应,则转移电子的物质的量为5 mol
参与该反应,则转移电子的物质的量为5 mol
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 明矾净水原理是氢氧化铝胶粒能吸附水中杂质
B. 根据能否产生丁达尔效应将分散系分为胶体、溶液和浊液
C. 面粉厂、水泥厂“电泳除尘”是利用了胶体带电
D. 利用过滤操作可以提纯蛋白质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述,正确的是
A. 构成原电池的正极和负极必须是两种活泼性不同的金属
B. 原电池是将化学能转变为电能的装置
C. 在原电池中,电子流出的一极是负极,该电极被还原
D. 原电池放电时,电流的方向是从负极到正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠(NaA)可作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2。已知25 ℃时,HA、H2CO3的电离平衡常数分别为 K=6.25×10-5、 K1=4.3×10-7,则下列说法正确的是(不考虑饮料中其他成分) ( )
A.提高CO2充气压力,饮料中c(A-)不变
B.当pH为5.0时,饮料中![]()
C.相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
D.结合H+的能力:A-> HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.01mol NH4Cl和0.002mol NaOH溶于水配成1L混合溶液,
(1)混合溶液中共有 种(填数字)不同的粒子。
(2)这些粒子中,浓度为0.01mol/L的是 ,浓度为0.002mol/L的是 。
(3)物质的量之和为0.01mol的两种粒子是__________________。
(4) 和 两种粒子数量之和比OH-多0.008mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列8种物质,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
①甲烷 ②苯 ③聚乙烯 ④1,3-丁二烯 ⑤2-丁炔 ⑥邻二甲苯 ⑦乙醛 ⑧环己烯
A. ③④⑤⑧ B. ④⑤⑦⑧ C. ④⑤⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些资料认为:NO、NO2不能与Na2O2反应。某小组学生提出质疑,他们从理论上分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设:
假设Ⅰ.过氧化钠氧化二氧化氮
假设Ⅱ.二氧化氮氧化过氧化钠
(1)小组甲同学设计实验如下:
①试管A中反应的化学方程式是 。
②待试管B中收集满气体,向试管B中加入适量 Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的小木条迅速伸进试管内,发现木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的。为准确达到实验目的,需在A、B之间增加一个装置,该装置的作用是 。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;余烬木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的方程式是 。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:①2NO+Na2O2=2NaNO2
②6NaNO2+3H2SO4=3Na2SO4+2HNO3+4NO↑+2H2O;
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
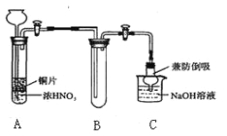
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。

①B中观察到的主要现象是 ,F装置的作用是 。
②在反应前,打开弹簧夹,通入一段时间N2,目的是 。
③充分反应后,检验D装置中反应产物的实验方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是 ( )
A.某特定反应的平衡常数仅是温度的函数
B.化学平衡发生移动,平衡常数必发生变化
C.其他条件一定时,平衡常数发生变化,化学平衡必定发生移动
D.催化剂不能改变平衡常数的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中正确的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com