
【题目】下列叙述中,不正确的是 ( )
A.某特定反应的平衡常数仅是温度的函数
B.化学平衡发生移动,平衡常数必发生变化
C.其他条件一定时,平衡常数发生变化,化学平衡必定发生移动
D.催化剂不能改变平衡常数的大小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某吸水材料与聚酯纤维都是重要的化工原料。它们的合成路线如图所示:
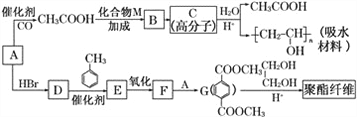
已知:①A由C、H、O三种元素组成,相对分子质量为32。
②RCOOR′+R″OH![]() RCOOR″+R′OH(R、R′、R″代表烃基)。
RCOOR″+R′OH(R、R′、R″代表烃基)。
请回答下列问题:
(1) A的结构简式是____________________。
(2)B中的官能团名称是______________________。
(3)D→E的反应类型是______________。
(4)①乙酸与化合物M反应的化学方程式是_________________________________
②G→聚酯纤维的化学方程式是______________。
(5) E的名称是___________。
(6) G的同分异构体有多种,满足下列条件的共有_____种。
①苯环上只有两个取代基;
② 1 mol该物质与足量的NaHCO3溶液反应生成2 mol CO2。
(7) 写出由![]() 合成
合成![]() 的流程图(注明反应条件)________。
的流程图(注明反应条件)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,RO![]() 与R-可发生反应:RO
与R-可发生反应:RO![]() +5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
+5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
A. R2在常温常压下一定是气体 B. RO![]() 中的R只能被还原
中的R只能被还原
C. 元素R位于周期表中第ⅤA族 D. 若1 mol RO![]() 参与该反应,则转移电子的物质的量为5 mol
参与该反应,则转移电子的物质的量为5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn(OH)2可溶于氨水生成[Zn(NH3)4]2+: Zn(OH)2+4NH3·H2O=Zn(NH3)4]2++4H2O+2OH-
(1)原子序数比Zn元素小1的元素符号为____,该元素原子基态核外电子排布式为______。
(2)NH3、H2O的沸点均高于同族元素氢化物的沸点,是因为________。
(3)NH3中N原子轨道的杂化类型是______。
(4)与H2O分子互为等电子体的分子为_____。
(5)闪锌矿是一种自然界含Zn元素的矿物,其晶体结构属于立方晶体(如右图所示),则在立方ZnS晶体结构中S2-的配位数为________。Zn2+的分数坐标为(l/4,l/4,l/4)、(3/4, 3/4,l/4)、(3/4,l/4,3/4)、(1/4,3/4,3/4),则S2-的分数坐标为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,将2mol X、2mol Y分别充入到不同体积的容器中,发生反应:X(g)+Y (g)![]() mZ(g) ΔH,所得Z的平衡浓度如表所示,下列说法正确的是( )
mZ(g) ΔH,所得Z的平衡浓度如表所示,下列说法正确的是( )
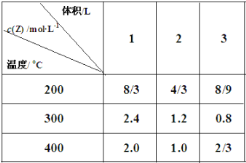
A.m=2 ,ΔH>0
B.300℃时,该反应平衡常数 K=9
C.在3L容器中进行反应,达到平衡的时间:400℃>200℃
D.200℃,2L容器中反应达平衡后,再充入2 mol Z,平衡时 Z 的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)
Ⅰ.某温度下,0.1 mol/L的氢硫酸溶液中存在平衡:
①H2S(aq)![]() H+(aq)+HS-(aq);②HS-(aq)
H+(aq)+HS-(aq);②HS-(aq)![]() H+(aq)+S2-(aq);
H+(aq)+S2-(aq);
(1)氢硫酸溶液中存在的离子有 。(不完整不给分)
(2)若向H2S溶液中( )
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH增大
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH的电离平衡常数表达式 。
(2)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为 。
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是 。

Ⅲ.在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH![]() )=c(Cl-),则溶液显 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
)=c(Cl-),则溶液显 性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,某无色溶液中,由水电离出的c(H+)=1×10-14 mol/L,则该溶液中,一定能大量共存的离子是( )
A.K+、Na+、MnO4-、SO42- B.Na+、CO32-、AlO2-、Cl-
C.K+、Na+、Cl-、Br- D.K+、Cl-、Ba2+、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物说法不正确的是
A. CH3CH(OH)CH2COOH系统命名法命名3-羟基丁酸
B. 四苯基乙烯(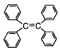 )中所有碳原子一定处于同一平面
)中所有碳原子一定处于同一平面
C. lmol 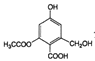 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol
分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol
D. 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图是由4个碳原子结合成的5种有机物(氢原子没有画出)

(1)写出有机物(a)的习惯命名法的名称______________ 。
(2)有机物(a)有一种同分异构体,写出其结构简式______________ 。
(3)上述有机物中与(c)互为同分异构体的是___________(填代号)。
(4)上述有机物中不能与溴水反应使其褪色的有______________(填代号)。
Ⅱ.写出烷烃C5H12的同分异构体中沸点最低的一种的结构简式_____________。
若此烷烃的一氯代物分子中含有两个-CH3,两个-CH2-,一个![]() 和一个-Cl,它的可能结构有四种,请写出它们的结构简式:_________________。
和一个-Cl,它的可能结构有四种,请写出它们的结构简式:_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com