
| ���� | �¶�/�� | ���ʵ���ʼŨ��/mol•L-1 | ���ʵ�ƽ��Ũ��/mol•L-1 | ||
| c��H2�� | c��CO�� | c��CH3OH�� | c��CH3OH�� | ||
| �� | 400 | 0.20 | 0.10 | 0 | 0.080 |
| �� | 400 | 0.40 | 0.20 | 0 | |
| �� | 500 | 0 | 0 | 0.10 | 0.025 |
| A�� | �÷�Ӧ������Ӧ���� | |
| B�� | �ﵽƽ��ʱ���������з�Ӧ��ת���ʱ��������еĴ� | |
| C�� | �ﵽƽ��ʱ����������c��H2��������������c��H2�������� | |
| D�� | �ﵽƽ��ʱ���������еķ�Ӧ���ʱ��������еĴ� |
���� �ԱȢ����¶���ͬ��0.1mol/L��CH3OH�൱��0.20mol/L��H2��0.1mol/L��CO��Ϊ��Чƽ�⣬�����¶Ƚϸߣ�ƽ��ʱCH3OH�ϵͣ�˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ���ԱȢ�����ͬ�¶��·�Ӧ������Ũ�Ƚϴ��ɷ���ʽ��֪������Ũ�ȣ�ƽ�������ƶ����Դ˽����⣮
��� �⣺A���ԱȢ����¶���ͬ��0.1mol/L��CH3OH�൱��0.20mol/L��H2��0.1mol/L��CO��Ϊ��Чƽ�⣬�����¶Ƚϸߣ�ƽ��ʱCH3OH�ϵͣ�˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����A��ȷ��
B���ԱȢ�����ͬ�¶��·�Ӧ������Ũ�Ƚϴ��ɷ���ʽ2H2��g��+CO��g��?CH3OH��g����֪������Ũ�ȣ�ƽ�������ƶ����÷�Ӧ����Ϊ�����С�ķ�Ӧ������Ũ��ת���ʻ��������������з�Ӧ��ת���ʱ��������е�С����B����
C����Ũ�Ƚϴ��¶Ƚϸߣ�����Ũ��ƽ�������ƶ��������¶�ƽ�������ƶ������ת���ʽ��ͣ������൱����ʼC��H2��Ϊ���һ�룬ƽ��ʱ����C��H2��С�ڢ��е���������C����
D���ԱȢ��¶Ƚϸߣ�Ũ���൱�������¶ȣ���Ӧ��������D��ȷ��
��ѡAD��
���� ���⿼�黯ѧ��Ӧ���ʵ�Ӱ�죬�漰��Чƽ�����⣬Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��Ŀ�ѶȲ����״�������ʱע����շ�Ӧ���ص��Լ�ƽ���Ӱ�����أ�


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
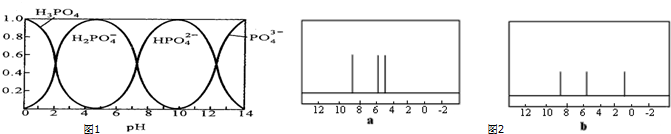
 ������N�к���2������̼ԭ�ӣ�
������N�к���2������̼ԭ�ӣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
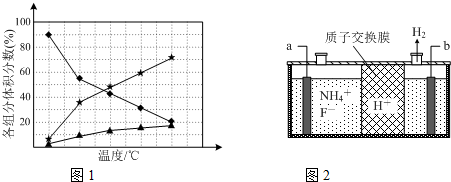
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 3s2��3s23p5 | B�� | 2s22p2��2s22p4 | C�� | 1s1��3s23p4 | D�� | 3s23p4��2s22p4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
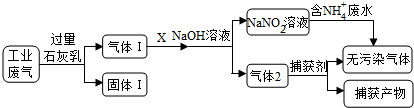
| A�� | ���������Ҫ����Ca��OH��2��CaCO3��CaSO3 | |
| B�� | X�����ǿ������������ | |
| C�� | ������������������Ҫ��CO | |
| D�� | ������NH4+��ˮʱ��������Ӧ�����ӷ���ʽΪ��NH4++NO2-=N2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
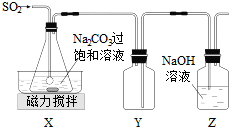
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������Һ��Ӧ��Cl2+2OH-�TCl-+ClO-+H2O | |
| B�� | ̼��Ƽ��������У�CO32-+2H+�TH2O+CO2�� | |
| C�� | ����FeCl3��Һ��Ӧ��Fe+Fe3+�T2Fe2+ | |
| D�� | ��MgCl2��Һ���백ˮ��Mg2++2OH-�TMg��OH��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
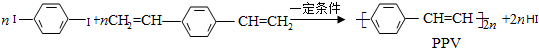
| A�� | PPV�Ǿ۱���Ȳ | |
| B�� | �÷�ӦΪ���۷�Ӧ | |
| C�� | PPV��۱���ϩ����С�ṹ��Ԫ�����ͬ | |
| D�� | 1 mol 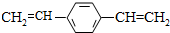 ������2 mol H2������Ӧ ������2 mol H2������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڵ��Ȼ�þ | B�� | ����ʳ��ˮ | C�� | ��̬������̼ | D�� | Һ̬�Ȼ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com