
【题目】已知氨基酸可发生如下反应:
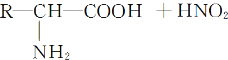
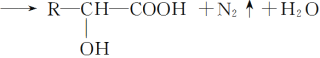
且已知:D、E的相对分子质量分别为162和144,可发生如下物质转化关系,如下图所示:
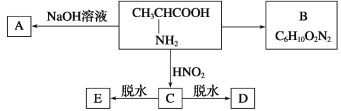
(1)写出C中所含官能团的名称:________________________
(2)写出B、D的结构简式:B____________,D________________________。
(3)写出C→E的化学方程式:_______________________________________。
(4)写出C发生缩聚反应的化学方程式:_______________________________________。
【答案】羟基、羧基 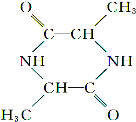
![]()
 n
n![]()
![]()
![]() +(n-1)H2O
+(n-1)H2O
【解析】
氨基酸能发生缩合反应,脱去一个H2O分子时,-COOH脱去-OH,-NH2脱去-H,发生缩聚反应生成多肽,结合B的分子式,两个丙氨酸分子间脱去2个H2O分子可生成B为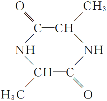 ;由题中所给信息可总结出:在HNO2作用下,氨基酸中的-NH2可转变成-OH,可得C为
;由题中所给信息可总结出:在HNO2作用下,氨基酸中的-NH2可转变成-OH,可得C为![]() ;由于C中含有-COOH和-OH,可以发生脱水反应生成D与E,而D、E的相对分子质量分别为162和144,故C脱去一个水分子可得D为
;由于C中含有-COOH和-OH,可以发生脱水反应生成D与E,而D、E的相对分子质量分别为162和144,故C脱去一个水分子可得D为![]() ,C脱去两个水分子可得E为
,C脱去两个水分子可得E为 ;丙氨酸与氢氧化钠发生中和反应生成A为CH3CH(NH2)COONa,据此分析解答。
;丙氨酸与氢氧化钠发生中和反应生成A为CH3CH(NH2)COONa,据此分析解答。
(1)由上述分析可知,C为![]() ,所含官能团有羟基和羧基,故答案为:羟基、羧基;
,所含官能团有羟基和羧基,故答案为:羟基、羧基;
(2)B的结构简式为 ,D的结构简式为
,D的结构简式为![]() ;
;
(3)C→E的化学方程式为: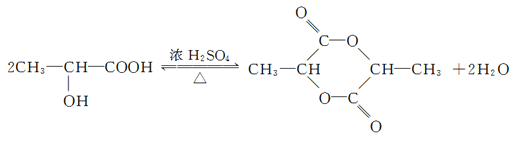 ;
;
(4)C发生缩聚反应的化学方程式为n![]()
![]()
![]() +(n-1)H2O,故答案为:n
+(n-1)H2O,故答案为:n![]()
![]()
![]() +(n-1)H2O。
+(n-1)H2O。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题。
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]()
(1)只含有离子键的是______(填序号,下同)
(2)含有共价键的离子化合物是______,其中含有非极性共价键的物质的电子式为______。
(3)属于共价化合物的是______。
(4)熔融状态下能导电的化合物是______。
(5)熔融状态下和固态时都能导电的物质是______。
(6)用电子式表示![]() 的形成过程:______。
的形成过程:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业是国民经济的支柱产业。下列生产过程中不涉及化学变化的是( )
A. 氮肥厂用氢气和氮气合成氨 B. 钢铁厂用热还原法冶炼铁
C. 硫酸厂用接触法生产硫酸 D. 炼油厂用分馏法生产汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状态下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为( )
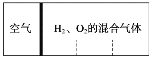
A. 2∶7B. 5∶4C. 4∶5D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是
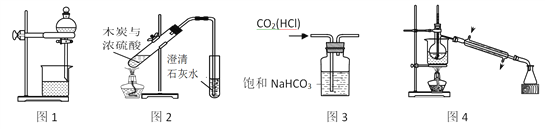
A. 图1用于分离酒精和水
B. 图2用于验证木炭与浓硫酸的反应产物中含有CO2
C. 图3用于除去CO2中的少量HCl
D. 图4用于制备蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
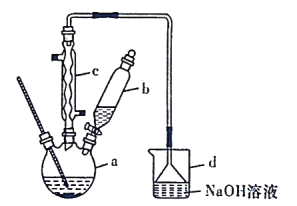
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g/cm3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解性 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在装置a中加入15mL无水苯和少量铁屑。在装置b中小心加入4.0mL液态溴。向装置a中滴入几滴溴,有白雾产生。继续滴加至液溴滴完。装置d的作用是吸收________和少量溴蒸汽。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是________________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入无水氯化钙的目的是________________________。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须的是________(填字母代号)。
A.重结晶 B.过滤
C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________(填字母代号)。
A.25mL B.50mL
C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧的烧渣(主要成分为Fe2O3、SiO2,不考虑其他杂质)制取绿矾(FeSO4·7H2O),流程如图:
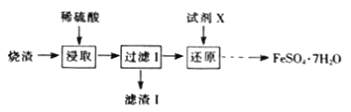
(1)滤渣Ⅰ的主要成分是___(填化学式)。
(2)还原时,试剂X若选用SO2,其反应后生成的阴离子是(填化学式)___。
(3)从还原后的溶液中得到产品,应进行的操作是___、___、过滤、洗涤、干燥。
(4)绿矾(FeSO4·7H2O)在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量。
步骤a:取10片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250.00mL溶液;
步骤b:取上述溶液25.00mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.1000mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应),发生的反应为:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O;
步骤c:重复“步骤b”2~3次,平均消耗KMnO4溶液20.00mL。该补血剂中亚铁离子的含量为___mg/片。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H(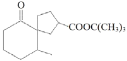 )是一种用于合成健脾,祛风,散寒药物的中间体,其合成路线如下:
)是一种用于合成健脾,祛风,散寒药物的中间体,其合成路线如下:

已知:①![]()
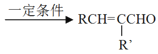 +H2O(R,
+H2O(R,![]() 是H或烃基)
是H或烃基)
②![]()
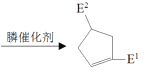 (
(![]() 可以是
可以是![]() 或
或![]() )
)
回答下列问题:
(1)A含有的官能团是__________________________________;
(2)B的结构简式为__________________________________;
(3)将下列B→C的多步反应流程图补充完整(标明反应条件):
_____________________________________________;
(4)由C和D生成E的化学方程式为_______________________________________;
(5)下列说法正确的是_______________________;
a.物质D的核磁共振氢谱有2组吸收峰;
b.物质F可与FeCl3溶液发生显色反应;
c.G→H的反应为加成反应;
(6)E和F反应生成G的化学方程式为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com