
| A. | 1L溶液中含有0.3NA个K+离子 | |
| B. | 1L溶液中含有K+和SO42-离子总数为0.9NA | |
| C. | 2L溶液中含K+的物质的量浓度为1.2mol/L | |
| D. | 2L溶液中含0.6NA个SO42-离子 |
分析 A.根据n=cV计算硫酸钾的物质的量,每摩尔硫酸钾含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
B.根据n=cV计算硫酸钾的物质的量,每摩尔硫酸钾含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
C.每摩尔硫酸钾含有2mol钾离子,钾离子的浓度为硫酸钾的2倍;
D.溶液是均一的,每摩尔硫酸钾含有1mol硫酸根,再根据N=nNA计算离子的数目.
解答 解:A.1L溶液中含有K+离子数为1L×0.3mol/L×2×NA=0.6NA,故A错误;
B.1L溶液中所含K+、SO42-总数为1L×0.3mol/L×3×NA=0.9NA,故B正确;
C.0.3mol/L K2SO4溶液,每摩尔硫酸钾含有2mol钾离子,钾离子的浓度为硫酸钾的2倍,所以K+离子浓度是0.6mol/L,故C错误;
D.溶液是均一的,每摩尔硫酸钾含有1mol硫酸根,2L溶液中含有SO42-离子=2L×0.3mol/L×1×NA=0.6NA,故D正确.
故选AC.
点评 本题考查溶液物质的量浓度,比较基础,注意溶液是均一的,浓度与体积无关,注意离子数和溶质微粒碱的计算.


科目:高中化学 来源: 题型:选择题
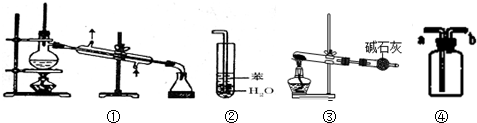
| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,防止倒吸 | |
| C. | 以KClO3 为原料,装置③可用于制备少量O2 | |
| D. | 装置④a进口可收集H2、CO 等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q2=$\frac{{Q}_{1}}{2}$ | B. | Q2>$\frac{{Q}_{1}}{2}$ | C. | Q2<Q1<Q | D. | Q=Q1>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的非金属性强弱顺序为R>W>Y | |
| B. | R与其他三种元素均能形成共价化化物 | |
| C. | 简单氢化物的热稳定性强弱顺序为R>Y>W | |
| D. | 原子半径大小顺序为r(W)>r(R)>r(X)>r(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用干燥的pH试纸检验CO2 | |
| B. | 用干燥的红色石蕊试纸检验NH3 | |
| C. | SO2能使湿润的品红试纸褪色 | |
| D. | 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
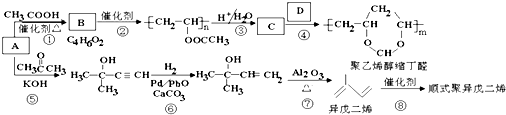
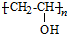 、CH3CH2CH2CHO.
、CH3CH2CH2CHO.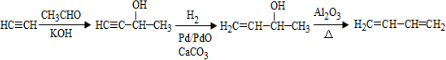 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
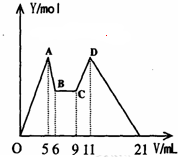 在氯化铝和氯化镁的混合溶液中,向其中滴加a mLC1mol•L-1 NaOH之后,改成滴加C2mol•L-1HCl,所得沉淀Y(mol)与试剂总体积V(mL)间的关系如右图所示.则所加入NaOH溶液的体积为( )
在氯化铝和氯化镁的混合溶液中,向其中滴加a mLC1mol•L-1 NaOH之后,改成滴加C2mol•L-1HCl,所得沉淀Y(mol)与试剂总体积V(mL)间的关系如右图所示.则所加入NaOH溶液的体积为( )| A. | 9mL | B. | 7.5mL | C. | 7ml | D. | 6mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 | |
| B. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{HCl(aq)}{→}$AlCl3 | |
| C. | NH3$\stackrel{O_{2}}{→}$NO$\stackrel{O_{2},H_{2}O}{→}$HNO3 | |
| D. | 饱和NaCl(aq)$\stackrel{NH_{3},CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
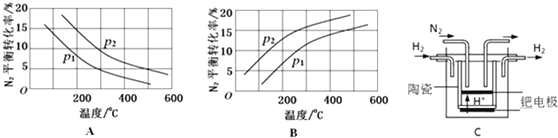
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com